Гонадотропные гормоны
Источник:
Клиническая фармакология по Гудману и Гилману, том 4.
Редактор: профессор А.Г. Гилман Изд.: Практика, 2006 год.
Содержание
- 1 Гонадотропные гормоны
- 2 Секреция гонадотропных гормонов
- 2.1 Регуляция секреции гонадолиберина
- 2.2 Механизм действия гонадолиберина
- 3 Механизм действия гонадотропных гормонов
- 4 Физиологические эффекты гонадотропных гормонов
- 5 Применение гонадолиберина и его аналогов
- 5.1 Диагностическое применение
- 5.2 Лечение бесплодия
- 5.3 Подавление секреции гонадотропных гормонов
- 6 Диагностическое применение гонадотропных гормонов
- 6.1 Тест на беременность
- 6.2 Определение времени овуляции
- 6.3 Диагностика расстройств репродуктивной функции
- 7 Лечебное применение гонадотропных гормонов
- 7.1 Женское бесплодие
- 7.2 Мужское бесплодие
- 7.3 Крипторхизм
- 8 Читайте также
- 9 Предупреждение
Гонадотропные гормоны [ править | править код ]
К гонадотропным гормонам гипофиза относят фолликул-стимулирующий гормон (ФСГ) и лютеинизирующий гормон (ЛГ). Хорионический гонадотропин (ХГ) тоже влияет на половые железы, но синтезируется плацентой. Эти три гормона вместе с тиреотропным гормоном (ТТГ) сходны по строению и образуют семейство гликопротеидных гормонов. Все они состоят из двух субъединиц: а-субъединица у всех одинаковая, а β-субъединицы различаются и обеспечивают специфическую активность. При этом β-субъединицы всех гормонов достаточно схожи, за исключением β-субъединицы ХГ, которая содержит дополнительный участок из 30 аминокислотных остатков на С-конце и несколько дополнительных углеводных остатков. Углеводные остатки увеличивают период полувыведения (Т1/2) этих гормонов в сыворотке, а также участвуют в их связывании с рецепторами. У человека ген, кодирующий β-субъединицу ФСГ, локализуется в сегменте 11р13, а β-субъединицу ЛГ — в сегменте 19ql2.32, по соседству по меньшей мере с 7 генами, кодирующими β-субъединицу ХГ. Ген, кодирующий а-субъединицу этих гормонов, локализуется в сегменте 6q21—q23.
Секреция гонадотропных гормонов [ править | править код ]
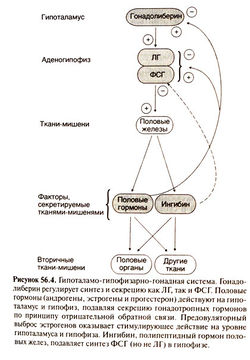
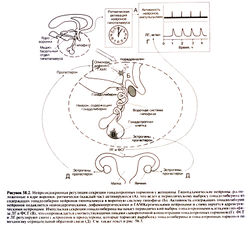
Регуляция секреции гонадотропных гормонов подробно описана в статье — половые гормоны. ЛГ и ФСГ синтезируются гонадотропными клетками, которые составляют около 20% секретирующих клеток аденогипофиза. ХГ, который обнаружен только у человека, приматов и лошадей, синтезируется клетками синцитиотрофобласта. Синтез ФСГ и ЛГ стимулируется гонадолиберином и регулируется по принципу обратной связи половыми гормонами (рис. 56.4 и 58.2).
Регуляция секреции гонадолиберина [ править | править код ]
Гонадолиберин — это гормон, который стимулирует синтез и секрецию ФСГ и ЛГ гонадотропными клетками аденогипофиза. Гонадолиберин образуется в результате протеолитического расщепления полипептида, содержащего 92 аминокислотных остатка, который Кодируется геном, расположенным в сегменте 8р21. Сам гонадолиберин представляет собой декапептид с амидной группой на С-конце и остатком пироглутаминовой кислоты на N-конце (табл. 56.3). Секреция гонадолиберина происходит импульсно в результате синхронизированной ритмической активности группы нейронов, расположенных в области ядра воронки. Активность этих нейронов начинается еще до рождения и продолжается примерно в течение года после него; затем она значительно снижается, вероятно, в результате тормозного действия ЦНС. Незадолго до начала полового развития тормозное действие ЦНС снижается, а частота и амплитуда импульсов секреции гонадолиберина увеличиваются, особенно сильно повышаясь во сне. По мере полового развития секреция гонадолиберина продолжает возрастать, пока не достигнет значений, характерных для взрослых. Импульсный характер секреции гонадолиберина необходим для нормального синтеза и секреции гонадотропных гормонов, секреция которых также происходит импульсно. Постоянное введение гонадолиберина приводит к десенситизации и снижению числа рецепторов гонадолиберина на гонадотропных клетках аденогипофиза. Это явление лежит в основе клинического применения аналогов гонадолиберина длительного действия, которые подавляют секрецию гонадотропных гормонов (см. ниже). После их введения секреция ЛГ и ФСГ кратковременно возрастает, но затем происходит десенситизация рецепторов, и секреция снижается.
Механизм действия гонадолиберина [ править | править код ]
Рецептор гонадолиберина относится к рецепторам, сопряженным с G-белками; его ген находится в сегменте 4q21. При связывании гонадолиберина или его аналогов с рецептором происходит активация белков Gq и GM, которые, в свою очередь, активируют фосфолипазу С, что приводит к увеличению внутриклеточной концентрации кальция. Это в итоге стимулирует синтез и секрецию ЛГ и ФСГ. Хотя цАМФ не принимает заметного участия в передаче сигнала от рецептора гонадолиберина, активация этого рецептора увеличивает активность аденилатциклазы. Рецепторы гонадолиберина присутствуют также в яичниках и яичках, однако их физиологическое значение остается неизвестным.
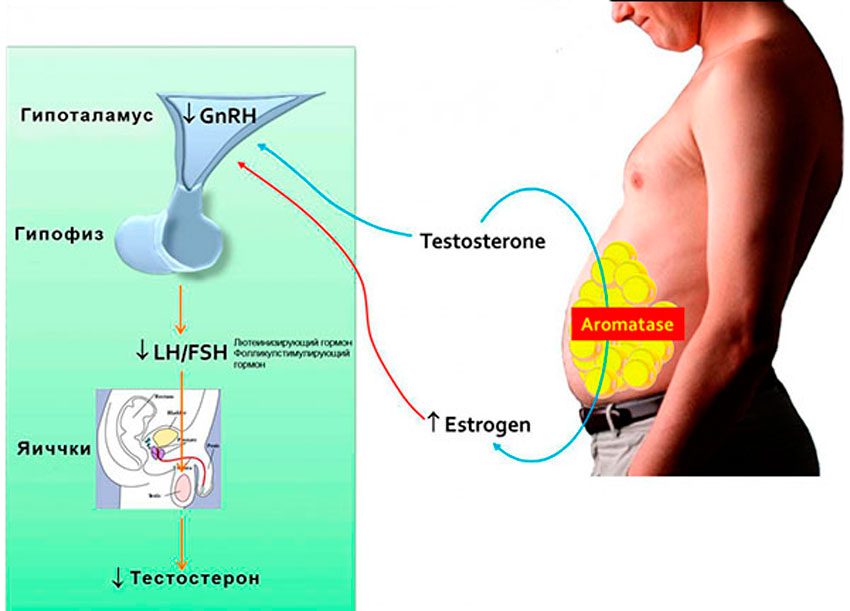
Половые гормоны также регулируют синтез ЛГ и ФСГ, воздействуя на гипоталамус и в меньшей степени — на гипофиз. Эта регуляция по-разному осуществляется у мужчин и женщин и зависит от возраста и фазы менструального цикла. У женщин низкие концентрации эстра-диола и прогестерона подавляют синтез гонадотропных гормонов за счет опосредованного опиоидами действия на нейроны, отвечающие за импульсную секрецию гонадолиберина. Однако длительное повышение концентрации эстрадиола действует по принципу положительной обратной связи, приводя к предовуляторному выбросу ЛГ. У мужчин синтез гонадотропных гормонов подавляется тестостероном, причем частично это обусловлено его прямым действием, а частично — превращением в эстрад иол.
Ингибин — пептидный гормон, образующийся в половых железах и играющий важную роль в регуляции секреции гонадотропных гормонов. Он синтезируется клетками гранулярного слоя фолликулов в яичниках и клетками Сертоли в яичках в ответ на стимуляцию гонадотропными гормонами и местными факторами роста. Ингибин действует непосредственно на гипофиз, избирательно подавляя секрецию ФСГ, но не Л Г. Ингибин относится к тому же семейству гликопротеидов, что и трансформирующий фактор роста |3 и фактор регрессии мюллеро-вых протоков.
Механизм действия гонадотропных гормонов [ править | править код ]
ЛГ и ХГ связываются с рецептором Л Г (ген этого рецептора находится в сегменте 2р21), а ФСГ — со своим рецептором (ген этого рецептора находится на длинном плече 2-й хромосомы). Оба рецептора сопряжены с G-белками и обладают большим внеклеточным гликозилированным доменом, ответственным за распознавание гормона. При связывании рецептора с лигандом G,-белок активирует аденилатциклазу, что ведет к повышению концентрации цАМФ. При высокой концентрации лиганда рецепторы через Gq-белок активируют также протеинкиназу С и увеличивают концентрацию кальция за счет активации фос-фолипазы С. Все или почти все эффекты гонадотропных гормонов можно воспроизвести введением в клетку аналогов цАМФ, поэтому значение протеинкиназы С и Са2+ во внутриклеточной передаче сигнала остается неясным.
Физиологические эффекты гонадотропных гормонов [ править | править код ]
ЛГ и ФСГ были названы в соответствии с их действием на яичники; функция этих гормонов у мужчин была изучена позднее. У мужчин ЛГ действует на клетки Лейдига, стимулируя синтез андрогенов, в основном тестостерона. Тестостерон обеспечивает половое влечение, развитие вторичных половых признаков и сперматогенез в извитых семенных канальцах. ФСГ действует на клетки Сертоли, стимулируя образование ими белков и питательных веществ, необходимых для созревания сперматозоидов.
У женщин действие ФСГ и ЛГ более сложно. ФСГ стимулирует рост и развитие фолликулов, а также индуцирует экспрессию гена рецептора ЛГ на текоцитах и клетках гранулярного слоя в яичниках. Кроме того, ФСГ активирует ароматазу в клетках гранулярного слоя, стимулируя синтез эстрадиола. ЛГ действует на текоциты, стимулируя образование в них андростендиона, основного предшественника эстрадиола в яичниках у женщин детородного возраста. ЛГ необходим также для разрыва фолликула при овуляции и для синтеза прогестерона желтым телом. Наконец, связывание ЛГ со своим рецептором на клетках гранулярного слоя увеличивает экспрессию гена рецептора ФСГ, что усиливает действие последнего.
Значение гонадотропных гормонов в регуляции функций половых органов отчетливо выявляется при мутациях генов самих гормонов или их рецепторов (Achermann and Jameson, 1999). У женщин с мутациями генов рецептора ФСГ или β-субъединицы самого ФСГ наблюдаются первичная аменорея и бесплодие, у них не созревают фолликулы, отсутствуют желтые тела и не развиваются молочные железы. Эти данные, а также эффективность ФСГ при некоторых формах бесплодия (см. ниже) красноречиво свидетельствуют о важной роли ФСГ в функционировании яичников. У мужчин при таких же мутациях уменьшен размер яичек и наблюдается олигозооспермия, хотя в некоторых случаях сохраняется фертильность.
Описан только один случай мутации с потерей функции гена β-субъединицы Л Г: у 46-летнего мужчины отсутствовало половое развитие, наблюдались гипоплазия клеток Лейдига и бесплодие. Наружные половые органы у него были развиты по мужскому типу, что, видимо, объясняется синтезом андрогенов под действием ХГ во время внутриутробного развития. Проявления мутаций с потерей функции гена рецептора ЛГ при мужском кариотипе варьируют от мужского гипогонадизма до развития наружных половых органов по женскому типу и отсутствия полового развития. Вероятно, вирилизации наружных половых органов не происходит из-за нарушения действия как ЛГ, так и ХГ во время внутриутробного развития. У женщин, гомозиготных по мутантным аллелям гена рецептора Л Г, отмечаются первичная аменорея или олигоменорея и бесплодие, а при гистологическом исследовании выявляются множественные кисты яичников.
Мутации, ведущие к постоянной активации рецептора ЛГ, возникают преимущественно у мужчин и наследуются аутосом-но-доминантно. Они ведут к преждевременному половому развитию из-за неуправляемого синтеза тестостерона во внутриутробном и в препубертатном периодах. При некоторых из этих мутаций высок риск опухолей яичка.
Применение гонадолиберина и его аналогов [ править | править код ]
В табл. 56.3 перечислены синтетические аналоги гонадолиберина, применяемые в клинике. Синтетический гонадолиберин называется гонадорелином. Замена аминокислотного остатка в положении 6 защищает аналоги гонадолиберина от протеолиза, а замена С-концевого остатка повышает сродство к рецептору. Такие аналоги обладают большей активностью и более длительным действием по сравнению с нативным гонадолиберином, Т1/2 которого составляет всего 2—4 мин.
Антагонисты гонадолиберина, в отличие от его аналогов длительного действия, не вызывают кратковременного повышения уровней гонадотропных гормонов в сыворотке. Современные антагонисты гонадолиберина, по-видимому, не приводят к местному и системному выбросу гистамина и анафилакгоидным реакциям, что ограничивало применение первых препаратов этой группы. Два антагониста гонадолиберина гаиреликс и цетрореликс применяют при искусственном оплодотворении для подавления выброса ЛГ во время стимуляции яичников. Ганиреликс доступен в США, а цетрореликс—только в Европе. Теоретически быстрое подавление выброса ЛГ дает возможность лучше контролировать стимуляцию яичников (см. ниже) и тем самым сокращает цикл искусственного оплодотворения. Однако практическую ценность этих препаратов при искусственном оплодотворении еще предстоит уточнить в клинических испытаниях.
Диагностическое применение [ править | править код ]
Один из препаратов гонадорелина (гонадорелина гидрохлорид) применяют для дифференциальной диагностики гипофизарного и гипоталамического поражения при вторичном гипогонадизме. Уровень ЛГ в сыворотке измеряют до введения гонадорелина в дозе 100 мкг п/к или в/в и в течение 2 ч (через 15,30,45,60 и 120 мин) после введения. Увеличение секреции ЛГ свидетельствует о наличии функционирующих гонадотропных клеток аденогипофиза. При длительном дефиците гонадолиберина чувствительность гонадотропных клеток к нему может снижаться, поэтому низкий уровень ЛГ при проведении пробы с гонадолиберином не обязательно говорит о поражении гипофиза. Пробу с гонадолиберином можно также использовать для дифференциальной диагностики истинного (связанного с секрецией гонадолиберина) и ложного преждевременного полового развития.
Лечение бесплодия [ править | править код ]
Другой препарат гонадорелина (гонадорелина ацетат) используют при нарушениях репродуктивной функции, связанных с дефицитом гонадолиберина. Препарат вводят в/в с помощью специального инфузионного насоса в импульсном режиме, имитирующем физиологическую секрецию, 2,5 мкг каждые 60—90 мин. Если овуляция не наступает, доза, вводимая за один импульс, может быть постепенно увеличена до 10 мкг. Принципы введения и дозы указаны в инструкции изготовителя. Гонадорелин реже, чем гонадотропные гормоны, вызывает многоплодную беременность. При лечении гона-дорелином не требуется столь тщательно контролировать уровень эстрогенов в сыворотке и проводить УЗИ яичников. Побочные реакции возникают редко, чаще всего развивается флебит в месте введения. При лечении гонадорелином у женщин восстанавливается физиологическая секреция половых гормонов, устанавливается менструальный цикл и происходит овуляция. Однако из-за технической сложности этот метод лечения применяют только в специализированных клиниках (Hayes et al., 1998).
При бесплодии у мужчин с помощью гонадорелина можно добиться роста яичек, нормальной секреции половых гормонов и сперматогенеза. Однако метод относительно дорог и требует постоянного ношения инфузионного насоса. К тому же гонадорелин не одобрен ФДА для лечения мужского бесплодия. Поэтому обычно предпочтение отдают гонадотропным гормонам.
Аналоги гонадолиберина длительного действия применяют также при индукций овуляции. Эти препараты подавляют предовуляторный выброс ЛГ и предотвращают лютеинизацию неовулирующего фолликула. Разработано несколько схем лечения, при которых длительно или краткосрочно вводят аналоги гонадолиберина совместно с гонадотропными гормонами, обеспечивающими созревание фолликула (см. ниже), а затем для индукции овуляции назначают ХГ (Lunenfeld, 1999).
Подавление секреции гонадотропных гормонов [ править | править код ]
Как уже говорилось, аналоги гонадолиберина длительного действия ведут к десенситизации рецепторов гонадолиберина, в результате чего секреция гонадотропных, а соответственно и половых, гормонов резко снижается. Такая «медикаментозная кастрация» оказалась очень удобной в тех случаях, когда нужно сократить выработку половых гормонов. Очевидное показание к подобному лечению — истинное преждевременное половое развитие у детей, при котором длительное введение аналогов гонадолиберина очень эффективно и почти не сопровождается побочными реакциями.
Аналоги гонадолиберина длительного действия используют для паллиативного лечения гормонально-зависимых опухолей (например, рака предстательной или молочной желез); поскольку в начале лечения эти препараты резко усиливают секрецию половых гормонов, одновременно назначают препараты, нарушающие синтез или блокирующие действие половых гормонов. Кроме того, аналоги гонадолиберина длительного действия используют при других гормонально-зависимых заболеваниях (эндометриозе, миоме матки и острой перемежающейся порфирии). Наконец, для медикаментозной кастрации при таких психических расстройствах, как педофилия, когда очень высок риск несоблюдения врачебных предписаний, особенно удобен гозерелин, который вводят в дозе 10,8 мг п/к 1 раз в 3 мес.
Аналоги гонадолиберина длительного действия в целом хорошо переносятся и вызывают вполне предсказуемые побочные эффекты, обусловленные нарушением синтеза половых гормонов: приливы, сухость влагалища, атрофический вагинит, снижение плотности костной ткани. В связи с этим при таких заболеваниях, как эндометриоз и миома матки, лечение обычно продолжают не более 6 мес или дополнительно назначают эстрогены для поддержания плотности костной ткани.
Диагностическое применение гонадотропных гормонов [ править | править код ]
Тест на беременность [ править | править код ]
В крови и моче беременных в больших количествах присутствует ХГ, поэтому в качестве теста на беременность можно использовать иммунохимическое выявление β-субъединицы ХГ. Качественное определение β-субъединицы ХГ в моче лежит в основе тестов на беременность для домашнего применения, продаваемых в США без рецепта. Эти тесты позволяют быстро выявить беременность уже через несколько дней после задержки менструации.
Количественное определение концентрации ХГ в плазме в клинических и научных целях проводят с помощью РИА. Обычно это делают для оценки прогрессирования беременности, а также при подозрении на внематочную беременность, пузырный занос или хориокарциному.
Определение времени овуляции [ править | править код ]
Овуляция происходит через 36 ч после начала выброса ЛГ и через 10—12 ч после достижения пика его концентрации. Поэтому по концентрации ЛГ в моче можно предсказать время овуляции. Для домашнего использования выпускают наборы, позволяющие при помощи специфических антител полуколичественно оценить уровень ЛГ в моче. Тест проводят каждые 12 или 24 ч начиная с 11 -го дня цикла (при 28-дневном цикле) и по увеличению уровня Л Г определяют предполагаемое время овуляции. Это дает возможность повысить вероятность зачатия путем правильного выбора времени для полового сношения.
Диагностика расстройств репродуктивной функции [ править | править код ]
Количественное измерение уровня ФСГ и ЛГ в плазме методом РИА (по уровню β-субъединиц) используют для диагностики некоторых нарушений репродуктивной функции. Низкие или неопределяемые уровни ФСГ и ЛГ свидетельствуют о вторичном гипогонадизме и о поражении гипофиза или гипоталамуса. При первичном гипогонадизме уровни этих гормонов, наоборот, высокие. При аменорее у женщин или задержке полового развития у мужчин и женщин определение уровня ФСГ и ЛГ позволяет отличить поражение половых желез от поражения гипоталамо-гипофизарной системы.
По уровню ФСГ на 3-й день менструального цикла можно судить о фертильности. Даже при нормальном менструальном цикле уровень ФСГ 15 МЕ/мл и более говорит о низкой фертильности, и успех искусственного оплодотворения при этом маловероятен (см. ниже).
Проба с ХГ используется у мужчин для оценки функции клеток Лейдига по степени стимуляции синтеза тестостерона. Эту пробу попользуют при подозрении на нарушение функции клеток Лейдига (например, при задержке полового развития). Уровень тестостерона в сыворотке определяют после нескольких инъекций ХГ. Сниженная секреция тестостерона говорит о патологии клеток Лейдига, а нормальная — о поражении гипоталамо-гипофизарной системы.
Лечебное применение гонадотропных гормонов [ править | править код ]
Изначально гонадотропные гормоны для клинического применения получали из человеческих гипофизов (трупный материал) и из мочи женщин. Препараты гипофиза сейчас не используют из-за риска передачи возбудителя болезни Крейтцфельдта—Якоба. Из мочи получают несколько препаратов. ХГ, который по действию аналогичен Л Г, получают из мочи беременных. Из мочи женщин в постменопаузе получают препарат менотропин, который содержит примерно одинаковые количества ЛГ и ФСГ, а также другие белки мочи. Поскольку менотропин относительно плохо очищен, во избежание аллергических реакций его вводят в/м. Другой препарат — урофоллитропин — представляет собой очищенный ФСГ, получаемый путем удаления ЛГ иммунологическими методами. Урофоллитропин сверхвысокой очистки получают при помощи моноклональных антител к ФСГ. Он очищен настолько, что его можно вводить п/к.
Методами генной инженерии получена линия клеток млекопитающих, синтезирующая а- и р-субъединицы ФСГ. Получающийся при этом рекомбинантный ФСГ близок по характеру гликозилирования к нативному ФСГ. Сегодня выпускается два препарата рекомбинантного ФСГ — фоллитропин а и фоллитропин Р; их углеводные структуры слегка различаются. Оба эти препарата вводят п/к, поскольку они намного чище препаратов, получаемых из мочи, и значительно лучше стандартизованы. Рекомбинантные препараты стоят намного дороже нативных, однако данных за то, что они эффективнее или реже вызывают такие побочные реакции, как синдром гиперстимуляции яичников, пока нет. Вероятно, в будущем методами генной инженерии удастся получить аналоги гонадотропных гормонов более длительного действия и с более высокой активностью.
Женское бесплодие [ править | править код ]
Бесплодием страдают около 10% супружеских пар детородного возраста. Для лечения бесплодия все шире применяют гонадотропные гормоны (Vollenhoven and Healy, 1998); часто их используют при искусственном оплодотворении. Хотя основным показанием к их назначению служит хроническая ановуляция в результате вторичного гипогонадизма (группа 1 по классификации ВОЗ), гонадотропные гормоны используют и для индукции овуляции при синдроме поликистозных яичников (группа II по классификации ВОЗ) в том случае, когда кломифен неэффективен (гл. 58). Кроме того, гонадотропные гормоны применяют при бесплодии на фоне нормальной овуляции, хотя в этих случаях сначала пробуют лечение кломифеном. Назначать гонадотропные гормоны должны врачи с достаточным опытом лечения бесплодия и эндокринных расстройств.
При хронической ановуляции назначение одного ФСГ в большинстве случаев вызывает овуляцию. Обычно ФСГ назначают в дозе 75 МЕ/сут в течение первых 6—7 дней цикла, после чего при помощи влагалищного УЗИ оценивают число и размер созревающих фолликулов. УЗИ обычно проводят каждые 2—3 сут. Созревание фолликула считается адекватным, если обнаружен фолликул диаметром 18 мм. Если обнаружено три и более фолликула диаметром более 16 мм, ФСГ отменяют из-за опасности синдрома гиперстимуляции яичников (см. ниже) и применяют барьерные методы контрацепции для предотвращения многоплодной беременности. Определяют также концентрацию эстрадиола, которая должна находиться в диапазоне 500—1500 пг/мл. Более низкие значения указывают на недостаточную стимуляцию яичников, а более высокие — на опасность синдрома гиперстимуляции яичников. При недостаточной стимуляции яичников доза ФСГ может быть увеличена до 150 МЕ/сут.
Для завершения созревания фолликула и индукции овуляции на следующий день после отмены ФСГ назначают ХГ в дозе 5000—10 000 ME. При лечении гонадотропными гормонами в 10—20% случаев развивается многоплодная беременность, что связано с развитием нескольких третичных фолликулов и выходом нескольких яйцеклеток.
Гонадотропные гормоны используют при искусственном оплодотворении, в том числе при экстракорпоральном оплодотворении и микроинъекции сперматозоидов в цитоплазму яйцеклетки. С помощью ФСГ стимулируют развитие фолликулов, а для окончательного их созревания назначают ХГ, после чего зрелые яйцеклетки извлекают из третичных фолликулов хирургическим путем. Затем производят экстракорпоральное оплодотворение полученных яйцеклеток с помощью спермы или микроинъекции сперматозоидов в цитоплазму яйцеклетки. Эмбрионы переносят в полость матки или в маточную трубу. При искусственном оплодотворении риск многоплодной беременности зависит от числа перенесенных эмбрионов.
Помимо многоплодной беременности и ее возможных осложнений основным побочным эффектом гонадотропных гормонов является синдром гиперстимуляции яичников. Для этого синдрома характерно быстрое накопление жидкости в полости брюшины, плевральной полости и даже перикарде. Считается, что причина этого синдрома — выделение яичниками вещества, повышающего сосудистую проницаемость. Синдром гиперстимуляции яичников проявляется вздутием живота, болью в животе, тошнотой, рвотой, поносом, выраженным увеличением яичников, одышкой и олигурией. Синдром гиперстимуляции яичников может осложниться гиповолемией, водно-электролитными нарушениями, гемоперитонеумом, РДСВ, тромбоэмболиями и нарушением функции печени. При подозрении на развитие этого синдрома ХГ не назначают.
В некоторых исследованиях выдвигалось предположение, что гонадотропные гормоны увеличивают риск рака яичников, однако это осталось недоказанным. Важно отметить, что при стимуляции яичников ФСГ и менотропином не возрастает риск пороков развития у детей, рожденных из стимулированных яйцеклеток.
Мужское бесплодие [ править | править код ]
Лечение гонадотропными гормонами может быть эффективно, если причина бесплодия — их дефицит. Поскольку гонадотропные гормоны относительно дороги, а при длительном приеме может развиться резистентность к ним, обычно половое развитие стимулируют андрогенами, а гонадотропные гормоны применяют позже, для достижения собственно фертильности.
Лечение, как правило, начинают с введения ХГ в дозе 1000— 5000 ME в/м 3 раза в неделю до нормализации синтеза половых гормонов, о чем судят по клиническим признакам и уровню тестостерона в плазме. После этого дозу ХГ снижают до 2000 ME 2 раза в неделю и дополнительно вводят менотропин в дозе по 75—150 ME ЛГ и ФСГ 3 раза в неделю. Наиболее частое побочное действие гонадотропных гормонов — гинекомастия; она возникает почти у каждого третьего больного и, вероятно, связана с повышенной продукцией эстрогенов: Для созревания яичек требуется примерно 6 мес, а для установления полноценного сперматогенеза лечение приходится продолжать до 2 лет. После начала сперматогенеза или его возобновления (при вторичном гипогонадизме, возникшем после полового созревания) для продукции спермы достаточно поддерживающей терапии I ХГ. Как уже говорилось, все большую роль в лечении бесплодия, вероятно, будут играть рекомбинантные гонадотропные гормоны.
Крипторхизм [ править | править код ]
При крипторхизме одно или оба яичка не , опускаются в мошонку. У доношенных новорожденных мальчиков он встречается в 3% случаев, но с возрастом его распространенность заметно снижается. При крипторхизме нарушается сперматогенез и повышается риск герминогенных опухолей яичка. Поэтому считается, что низведение яичка в мошонку следует производить как 3 можно раньше, обычно в возрасте года и уж во всяком случае до 2 лет. Поскольку опущение яичка стимулируется андрогенами, в отсутствие анатомического препятствия можно использовать ХГ. Обычно назначают 6 инъекций ХГ по 500 МЕ/м2 в/м через день. При неэффективности такого лечения производят орхипексию.
Читайте также [ править | править код ]
Предупреждение [ править код ]

Источник статьи: http://sportwiki.to/%D0%93%D0%BE%D0%BD%D0%B0%D0%B4%D0%BE%D1%82%D1%80%D0%BE%D0%BF%D0%BD%D1%8B%D0%B5_%D0%B3%D0%BE%D1%80%D0%BC%D0%BE%D0%BD%D1%8B
Гормональный баланс на курсе ААС
Добавляя в свой рацион ААС, или, иначе говоря, синтетические мужские половые гормоны или их производные, стоит помнить о том, что наш организм стремится поддерживать гомеостаз, то есть находится в равновесии. Баланс половых гормонов не исключение. Наша гормональная система работает по принципу обратной связи. За повышением одного из гормонов следует повышение или, напротив, понижение другого, в зависимости от их природы и функции. Сразу оговорюсь, что речь пойдет преимущественно об ароматизирующихся препаратах, конкретнее – о тестостероне. В целом данная статья будет полезна всем, в том числе и тем, кто уже применяет ААС или еще собирается, для общего знакомства с основными гормонами и их функциями.
Половые гормоны можно поделить на две большие группы: андрогены (мужские) и эстрогены (женские).
Из группы андрогенов выделим для нас наиболее важные два гормона – это тестостерон и дигидротестостерон. Из группы эстрогенов – эстрадиол. Прогестерон
и пролактин относятся к другим группам женских половых гормонов, однако заострять внимание на том, к каким именно, в данной статье нет необходимости.
Тем не менее вышеперечисленные гормоны следует запомнить для себя, употребляя ААС, так как в основном именно с ними мы будем иметь дело, вторгаясь в нашу эндокринную систему. Считаю, что следует отнестись с должным вниманием к их содержанию в плазме крови. Почему это важно? Знание текущего положения дел в сфере гормонального баланса организма поможет избежать ряда побочных эффектов, связанных с завышенным показателем эстрадиола, пролактина и прогестерона, понять и оценить отклик вашей системы. Да и в целом, как и во многих других случаях, информированность не повредит. Постараемся лаконично рассмотреть основные мужские и женские гормоны, выявить некоторые закономерности и понять принцип их действия. Начнем.
Функция тестостерона
Тестостерон – основной мужской половой гормон, андроген. Отвечает за комплексное формирование мужчины. Тестостерон участвует в развитии вторичных половых признаков (мужской голос, растительность на теле, мужская конституция тела и т. д.), регулирует сперматогенез, половое поведение, а также оказывает влияние на азотистый и фосфорный обмен, ускоряет рост мышечной массы.
Фракции тестостерона
Свободный тестостерон – гормон, не связанный с белками альбумина и глобулина. Около 60 % тестостерона в крови связано с ГСПГ (глобулин, связывающий половые гормоны), другая же часть связана с альбумином. Примерно 4 % приходится на свободную часть тестостерона в организме.
Считается, что биологически активную форму представляет собой только свободный и связанный с белками альбумина тестостерон. Известно, что связанный тестостерон с ГСПГ защищен в системе циркуляции от протеолитической деградации, то есть от разрушения молекул гормона. Данные по поводу активности тестостерона, связанного с глобулином, весьма противоречивы. Нам же в контексте данной темы важно иметь общее представление о тестостероне, понимать различие свободного и общего.
Итак, коротко подведем итог: общий тестостерон – весь тестостерон в организме, в том числе и свободный, свободный же исключительно тот, что не связан с белками альбумина и глобулина.
Норма тестостерона для мужчин
Сразу поясню, что биологически активный тестостерон – тестостерон свободный + тестостерон, связанный с белками альбумина. Также отмечу, что у мужчин, которые регулярно занимаются с отягощениями, особенно в молодом возрасте, показатель может быть завышен, что не является патологическим отклонением.
Симптомы нехватки тестостерона:
- Снижение умственных способностей и памяти;
- Депрессии, раздражительность;
- Выпадение волос, отсутствие волосяного покрова;
- Увеличенное отложение жировой ткани;
- Эректильная дисфункция;
- Снижение либидо.
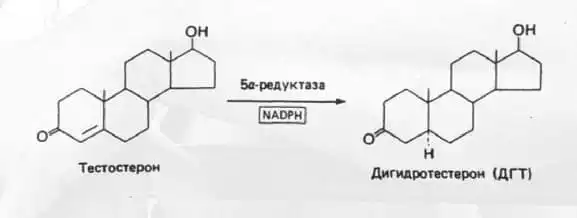
Конвертация тестостерона в дегидротестостерон
Молекула тестостерона и ДГТ
В той или иной степени, в зависимости от индивидуальных особенностей каждого, тестостерон в организме конвертируется в дигидротестостерон (сокращенно ДГТ). Происходит данный процесс под влиянием фермента 5-альфа-редуктазы. Если чуть углубиться в детали, то под воздействием вышеуказанного фермента к структуре молекулы тестостерона добавляется два атома водорода (отсюда и название «дигидротестостерон»), также удаляется 4–5-двойная связь тестостерона.
Дигидротестостерон занимает значимую позицию в организации и функционировании ЦНС.
Тут мы подходим к значению обозначенных преобразований. Созданный под воздействием перечисленных реакций стероид способен более успешно связываться
с андрогенными рецепторами, нежели сам тестостерон, что делает активность ДГТ в 3–4 раза сильнее, чем активность предшественника – тестостерона. Добавлю, что гормон прогестерон, который рассмотрим чуть позже, является антагонистом ДГТ. На повышение ДГТ организм может отреагировать логичным действием – повышением прогестерона
с целью избежать слишком сильной конверсии.
Действие ДГТ и побочные эффекты
Наиболее наступательно ДГТ проявляет себя в вопросах, связанных с простатой, кожным покровом, волосистой частью головы, печенью и различными регионами ЦНС. Связано это с тем, что 5-альфа-редуктаза локализируется преимущественно именно в этих тканях. Отсюда, к сожалению, всем известные побочные эффекты: облысение, гипертрофия простаты, сальных желез, как следствие – повышение жирности кожи и появление акне и т. д. Однако стоит понимать, что есть и существенные плюсы в сильной андрогенной активности ДГТ. Например, дигидротестостерон занимает значимую позицию в организации и функционировании ЦНС.
Большое количество нервных клеток имеют активные андрогенные рецепторы. На основе этого факта объясняется важность ДГТ в обеспечении полноценной работы ЦНС. Стоит понимать, что нормальная работа ЦНС – это не просто улучшение мыслительной деятельности, реакции, восстановления и т. д. Значительно улучшается взаимодействие между нервной системой и скелетными мышцами. Указанное взаимодействие называется нервно-мышечной связью,
о важности которой говорится весьма и весьма часто.
Могу лишь повториться и сказать, что необходимо чувствовать работу целевой мышечной группы на тренировке. Коротко можно упростить и выразить в следующей формуле: лучше чувствуем мышцу, лучше прорабатываем, лучше растем.
Нужна ли блокировка конверсии?
Блокировка конверсии тестостерона в ДГТ может привести к ухудшению результатов на курсе тестостерона, то есть к торможению роста мышечной массы и силы. Блокировка осуществляется при помощи добавления ингибитора 5-альфа- редуктазы, например, такой препарат, как финастерид. Однако скажу, что не стоит рассматривать ДГТ как исключительно негативный и ненужный гормон, он крайне важен в построении мышечной массы и увеличении силы.
Хочу добавить, что человек с повышенным фоном ДГТ не обязательно будет иметь какие-либо побочные эффекты, связанные с последним.
Во многом неприятные эффекты обуславливаются не только избыточной конверсией, но и индивидуальным количеством андрогенных рецепторов в тех или иных тканях.
Итак, мы выяснили, что ДГТ – это крайне сильный анаболический и андрогенный агент. При большом количестве андрогенных рецепторов в тех или иных тканях либо при завышенном фоне ДГТ гормон способен приводить к ряду побочных эффектов. Однако без него прогресс гипертрофии мышечных волокон и роста силы будет существенно ниже либо же вообще отсутствовать.
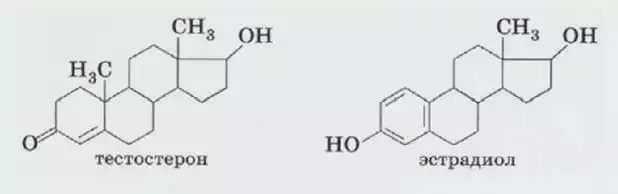
Тестостерон, ароматизация. Эстрадиол
Aроматизация
Под влиянием фермента ароматазы тестостерон способен превращаться в эстрадиол, отсюда и процесс, именуемый ароматизацией. Интересно, что молекулы тестостерона и эстрадиола отличаются совсем незначительно, а именно отсутствием одной метильной группы и нескольких атомов водорода. В мужском организме эстрадиол является производным тестостерона. А это значит, что, как правило, завышенный эстрадиол – это следствие повышенного тестостерона, исключая индивидуальные частные случаи, которые не являются правилом.
В избыточном количестве эстрадиол вредит мужчине, превращая его в женщину.
Давайте разберемся, что такое эстрадиол и зачем он нам. Эстрадиол, как мы определили в начале, относится к группе женских половых гормонов, эстрогенов. Данное гормональное вещество в организме мужчины выполняет ряд важнейших функций, например: активное участие в процессе секреции эякулята, улучшение кислородного обмена, регуляция функционирования нервной системы, увеличение свертываемости крови, стимулирование обмена веществ и т. д. Считается, что в избыточных количествах гормон способен приводить к таким побочным эффектам, как отложение жира по женскому типу, нервозность, снижение либидо и эректильная дисфункция, гинекомастия и т. д. Иными словами, для упрощения можно сказать, что в избыточном количестве эстрадиол вредит мужчине, превращая его в женщину.
Норма тестостерона для мужчин Эстрадиол (Е2) 3–70 пг/мл
Итак, мы выяснили, что избыток и недостаток эстрадиола вредны, необходима золотая середина.
Подавление ароматизации
Хотел бы остановиться подробнее на избыточном значении эстрадиола. Действительно, норма, обозначенная во многих медицинских источниках, находится в границе от 3 до 70 пг/мл. Но, как уже было сказано, эстрадиол – производное тестостерона, потому значение женского гормона будет выше границ нормы в случае употребления ААС, то есть тестостерона. И значит ли это, что в таком случае эстрадиол будет вреден и пора судорожно искать способ его понизить? Нет. Почему?
Дело не в количестве эстрадиола, а в его соотношении к тестостерону. В разных источниках описано по-разному, тем не менее наиболее часто встречаемые цифры – это 1:3–4, где 1 – тестостерон, 3–4 – эстрадиол.
Здесь, основываясь на личном опыте, опыте других, хочу сказать, что не всегда существует явная необходимость сбивать уровень эстрадиола. Многие также считают, что появление гинекомастии невозможно от завышенного фона эстрадиола. К сожалению, нельзя точно рассчитать значение и соотношение для конкретного человека, тем более для среднестатистического мужчины.
Также хочу сказать, что особенно первое время организм может реагировать на введение экзогенного тестостерона слишком большой ароматизацией, это нужно учитывать. Увы, какую-
то точную формулу дать не смогу, и, возможно, многие со мной не согласятся. Тем не менее считаю, что следует экспериментировать с дозировками ингибиторов ароматазы или с другими антиэстрогенными препаратами, тем самым выискать золотую середину для себя, ориентируясь на самочувствие и анализы. Помните, то, что подходит другим, не обязательно подойдет вам, и наоборот.
Способы подавления ароматизации
Особо много внимания данному разделу уделять не будем, но коротко пройдемся по наиболее популярным препаратам и способам.
Кломид действует на рецепторы эстрогенов в гипофизе и яичниках. Связывает рецепторы эстрогенов в гипофизе. Кломид разрывает механизм отрицательной обратной связи, то есть если обычно эстрогены, воздействуя на гипофиз, снижают выработку ФСГ и ЛГ последним, то при приеме кломида этого не происходит. На сам уровень эстрогенов в крови кломид не действует, точно так же не действует на уровень эстрогенов в крови, так как механизм его действия сводится к блокаде разных типов эстрогеновых рецепторов, в том числе и в гипофизе. Довольно-таки токсичный препарат. Также тамоксифен увеличивает количество рецепторов прогестерона.
Ингибиторы ароматазы (летрозол, анастрозол, эксеместан) – это класс лекарственных препаратов, предназначенных в первую очередь для снижения концентрации эстрогенов в крови. В отличие от тамоксифена и кломида, не блокирует рецепторы эстрогенов, воздействует непосредственно на ароматизацию, подавляя ее. Также применяется для повышения уровня собственного тестостерона и гонадотропных гормонов.
Снижение количества жировой ткани. Не стоит пренебрегать условием наличия большого или умеренно большого количества подкожного жира. Ведь
чем тучнее человек, тем сильнее ароматизация. Снижение процента подкожного жира значительно уменьшит ароматизацию. Также, как правило, на низкоуглеводных/безуглеводных диетах наблюдается снижение конверсии тестостерона в эстрадиол.
Пролактин и прогестерон
Прогестерон – женский половой гормон, прогестин. Иначе его называют «гормон беременности», потому что в женском организме, главным образом, именно он ответственен за поддержание беременности и регуляции менструального цикла. Мужчинам прогестерон также необходим, он выполняет ряд важных функций. Прогестерон является предшественником тестостерона и кортизола, регулирует работу ЦНС. Также прогестерон выступает в роли противовеса дигидротестостерону, снижая чрезмерную активность последнего.
Норма прогестерона у мужчин Прогестерон 0,5–6,0 нмоль/л
Допустимы колебания прогестерона, которые могут превышать до 100 % от референсных значений.
При завышенном уровне прогестерона с большим риском развивается атрофия яичек, бесплодие, подавляется либидо.
Интересно, что ранее существовала практика применения препаратов на основе данного гормона с целью подавления мужского полового влечения. Они вводились мужчинам-преступникам с целью снижения активности их половых инстинктов.
Тут, как и в других случаях, необходим рациональный подход к контролю прогестерона. В целом при использовании тестостерона прогестерон подниматься не должен в силу отсутствия прогестагенной активности тестостерона.
Существует мнение, что прогестерон занимает место No1 для развития гинекомастии. Почему? Если завышен прогестерон, то, во-первых, увеличивается количество рецепторов эстрадиола в тканях железы, а во-вторых, прогестерон сам по себе повышает пролактин. Поэтому даже при невысоком эстрадиоле может наблюдаться развитие гинекомастии.
Что может повлечь за собой повышение уровня прогестерона?
- Конверсия в дигидротестостерон;
- Прием ингибиторов ароматазы, «раскачка» эстрадиола;
- Низкий пролактин.
Пролактин
Пролактин – это пептидный гормон, состоящий из 199 аминокислот, который по своей структуре напоминает гормон роста, при этом выполняет другие функции,
хотя есть и некоторые функциональные сходства.
Функции пролактина в мужском организме сводятся к регуляции выделения
половых гормонов и сперматозоидов, также регуляции половой функции, иммуностимуляции и контролю над подвижностью сперматозоидов.
Также пролактин отвечает за лактацию. То есть он ответственен за развитие долек железы в груди и молочного протока от железы к соску. Если пролактин высокий, то сосок начинает расти в размерах.
Мужчинам прогестерон так же необходим, он выполняет ряд важных функций. Прогестерон является предшественником тестостерона и кортизола, регулирует работу ЦНС.
Сам по себе пролактин не вызывает гинекомастию у мужчин, но иногда он может способствовать ее развитию, так как усиливает действие эстрогенов, которые всегда присутствуют в крови мужского организма.
Вредит лишь завышенный пролактин. Многие любят съедать по полтаблетки достинекса или берголака (действующее вещество – каберголин) еженедельно без сданных анализов, что считаю неправильным. Вследствие этого пролактин падает до нулевых значений, а прогестерон повышается.
Норма пролактина Пролактин 53–360 мЕд\л
Вывод
Логика рассуждений сводится лишь к одному: не нужно слепо пытаться исправить что-либо, не зная даже что. Элементы системы организма взаимосвязаны между собой. Особенно гормональная система: если вы что-то понижаете, без следа это не остается. Поэтому, прежде чем «сбивать» уровень какого-то из гормонов, посмотрите на свои анализы. Помните всегда, что каждый организм и случай индивидуальны.
То, что у некоторых не повлечет за собой последствий, может повлечь их у других людей. На мой взгляд, путь человека, который занимается культуризмом, – это всегда путь экспериментатора, начиная от выбора продуктов, заканчивая выбором фармакологии. Никто лучше вашего организма вам совета не даст, поэтому прислушивайтесь к нему.
Источник статьи: http://ko4a.ru/gormonalnyj-balans-na-kurse-aas/
Фсг гормон в бодибилдинге
Гонадотропные гормоны
Содержание
Гонадотропные гормоны [ править | править код ]
К гонадотропным гормонам гипофиза относят фолликул-стимулирующий гормон (ФСГ) и лютеинизирующий гормон (ЛГ). Хорионический гонадотропин (ХГ) тоже влияет на половые железы, но синтезируется плацентой. Эти три гормона вместе с тиреотропным гормоном (ТТГ) сходны по строению и образуют семейство гликопротеидных гормонов. Все они состоят из двух субъединиц: а-субъединица у всех одинаковая, а β-субъединицы различаются и обеспечивают специфическую активность. При этом β-субъединицы всех гормонов достаточно схожи, за исключением β-субъединицы ХГ, которая содержит дополнительный участок из 30 аминокислотных остатков на С-конце и несколько дополнительных углеводных остатков. Углеводные остатки увеличивают период полувыведения (Т1/2) этих гормонов в сыворотке, а также участвуют в их связывании с рецепторами. У человека ген, кодирующий β-субъединицу ФСГ, локализуется в сегменте 11р13, а β-субъединицу ЛГ — в сегменте 19ql2.32, по соседству по меньшей мере с 7 генами, кодирующими β-субъединицу ХГ. Ген, кодирующий а-субъединицу этих гормонов, локализуется в сегменте 6q21—q23.
Секреция гонадотропных гормонов [ править | править код ]
Регуляция секреции гонадотропных гормонов подробно описана в статье — половые гормоны. ЛГ и ФСГ синтезируются гонадотропными клетками, которые составляют около 20% секретирующих клеток аденогипофиза. ХГ, который обнаружен только у человека, приматов и лошадей, синтезируется клетками синцитиотрофобласта. Синтез ФСГ и ЛГ стимулируется гонадолиберином и регулируется по принципу обратной связи половыми гормонами (рис. 56.4 и 58.2).
Регуляция секреции гонадолиберина [ править | править код ]
Гонадолиберин — это гормон, который стимулирует синтез и секрецию ФСГ и ЛГ гонадотропными клетками аденогипофиза. Гонадолиберин образуется в результате протеолитического расщепления полипептида, содержащего 92 аминокислотных остатка, который Кодируется геном, расположенным в сегменте 8р21. Сам гонадолиберин представляет собой декапептид с амидной группой на С-конце и остатком пироглутаминовой кислоты на N-конце (табл. 56.3). Секреция гонадолиберина происходит импульсно в результате синхронизированной ритмической активности группы нейронов, расположенных в области ядра воронки. Активность этих нейронов начинается еще до рождения и продолжается примерно в течение года после него; затем она значительно снижается, вероятно, в результате тормозного действия ЦНС. Незадолго до начала полового развития тормозное действие ЦНС снижается, а частота и амплитуда импульсов секреции гонадолиберина увеличиваются, особенно сильно повышаясь во сне. По мере полового развития секреция гонадолиберина продолжает возрастать, пока не достигнет значений, характерных для взрослых. Импульсный характер секреции гонадолиберина необходим для нормального синтеза и секреции гонадотропных гормонов, секреция которых также происходит импульсно. Постоянное введение гонадолиберина приводит к десенситизации и снижению числа рецепторов гонадолиберина на гонадотропных клетках аденогипофиза. Это явление лежит в основе клинического применения аналогов гонадолиберина длительного действия, которые подавляют секрецию гонадотропных гормонов (см. ниже). После их введения секреция ЛГ и ФСГ кратковременно возрастает, но затем происходит десенситизация рецепторов, и секреция снижается.
Механизм действия гонадолиберина [ править | править код ]
Рецептор гонадолиберина относится к рецепторам, сопряженным с G-белками; его ген находится в сегменте 4q21. При связывании гонадолиберина или его аналогов с рецептором происходит активация белков Gq и GM, которые, в свою очередь, активируют фосфолипазу С, что приводит к увеличению внутриклеточной концентрации кальция. Это в итоге стимулирует синтез и секрецию ЛГ и ФСГ. Хотя цАМФ не принимает заметного участия в передаче сигнала от рецептора гонадолиберина, активация этого рецептора увеличивает активность аденилатциклазы. Рецепторы гонадолиберина присутствуют также в яичниках и яичках, однако их физиологическое значение остается неизвестным.
Половые гормоны также регулируют синтез ЛГ и ФСГ, воздействуя на гипоталамус и в меньшей степени — на гипофиз. Эта регуляция по-разному осуществляется у мужчин и женщин и зависит от возраста и фазы менструального цикла. У женщин низкие концентрации эстра-диола и прогестерона подавляют синтез гонадотропных гормонов за счет опосредованного опиоидами действия на нейроны, отвечающие за импульсную секрецию гонадолиберина. Однако длительное повышение концентрации эстрадиола действует по принципу положительной обратной связи, приводя к предовуляторному выбросу ЛГ. У мужчин синтез гонадотропных гормонов подавляется тестостероном, причем частично это обусловлено его прямым действием, а частично — превращением в эстрад иол.
Ингибин — пептидный гормон, образующийся в половых железах и играющий важную роль в регуляции секреции гонадотропных гормонов. Он синтезируется клетками гранулярного слоя фолликулов в яичниках и клетками Сертоли в яичках в ответ на стимуляцию гонадотропными гормонами и местными факторами роста. Ингибин действует непосредственно на гипофиз, избирательно подавляя секрецию ФСГ, но не Л Г. Ингибин относится к тому же семейству гликопротеидов, что и трансформирующий фактор роста |3 и фактор регрессии мюллеро-вых протоков.
Механизм действия гонадотропных гормонов [ править | править код ]
ЛГ и ХГ связываются с рецептором Л Г (ген этого рецептора находится в сегменте 2р21), а ФСГ — со своим рецептором (ген этого рецептора находится на длинном плече 2-й хромосомы). Оба рецептора сопряжены с G-белками и обладают большим внеклеточным гликозилированным доменом, ответственным за распознавание гормона. При связывании рецептора с лигандом G,-белок активирует аденилатциклазу, что ведет к повышению концентрации цАМФ. При высокой концентрации лиганда рецепторы через Gq-белок активируют также протеинкиназу С и увеличивают концентрацию кальция за счет активации фос-фолипазы С. Все или почти все эффекты гонадотропных гормонов можно воспроизвести введением в клетку аналогов цАМФ, поэтому значение протеинкиназы С и Са2+ во внутриклеточной передаче сигнала остается неясным.
Физиологические эффекты гонадотропных гормонов [ править | править код ]
ЛГ и ФСГ были названы в соответствии с их действием на яичники; функция этих гормонов у мужчин была изучена позднее. У мужчин ЛГ действует на клетки Лейдига, стимулируя синтез андрогенов, в основном тестостерона. Тестостерон обеспечивает половое влечение, развитие вторичных половых признаков и сперматогенез в извитых семенных канальцах. ФСГ действует на клетки Сертоли, стимулируя образование ими белков и питательных веществ, необходимых для созревания сперматозоидов.
У женщин действие ФСГ и ЛГ более сложно. ФСГ стимулирует рост и развитие фолликулов, а также индуцирует экспрессию гена рецептора ЛГ на текоцитах и клетках гранулярного слоя в яичниках. Кроме того, ФСГ активирует ароматазу в клетках гранулярного слоя, стимулируя синтез эстрадиола. ЛГ действует на текоциты, стимулируя образование в них андростендиона, основного предшественника эстрадиола в яичниках у женщин детородного возраста. ЛГ необходим также для разрыва фолликула при овуляции и для синтеза прогестерона желтым телом. Наконец, связывание ЛГ со своим рецептором на клетках гранулярного слоя увеличивает экспрессию гена рецептора ФСГ, что усиливает действие последнего.
Значение гонадотропных гормонов в регуляции функций половых органов отчетливо выявляется при мутациях генов самих гормонов или их рецепторов (Achermann and Jameson, 1999). У женщин с мутациями генов рецептора ФСГ или β-субъединицы самого ФСГ наблюдаются первичная аменорея и бесплодие, у них не созревают фолликулы, отсутствуют желтые тела и не развиваются молочные железы. Эти данные, а также эффективность ФСГ при некоторых формах бесплодия (см. ниже) красноречиво свидетельствуют о важной роли ФСГ в функционировании яичников. У мужчин при таких же мутациях уменьшен размер яичек и наблюдается олигозооспермия, хотя в некоторых случаях сохраняется фертильность.
Описан только один случай мутации с потерей функции гена β-субъединицы Л Г: у 46-летнего мужчины отсутствовало половое развитие, наблюдались гипоплазия клеток Лейдига и бесплодие. Наружные половые органы у него были развиты по мужскому типу, что, видимо, объясняется синтезом андрогенов под действием ХГ во время внутриутробного развития. Проявления мутаций с потерей функции гена рецептора ЛГ при мужском кариотипе варьируют от мужского гипогонадизма до развития наружных половых органов по женскому типу и отсутствия полового развития. Вероятно, вирилизации наружных половых органов не происходит из-за нарушения действия как ЛГ, так и ХГ во время внутриутробного развития. У женщин, гомозиготных по мутантным аллелям гена рецептора Л Г, отмечаются первичная аменорея или олигоменорея и бесплодие, а при гистологическом исследовании выявляются множественные кисты яичников.
Мутации, ведущие к постоянной активации рецептора ЛГ, возникают преимущественно у мужчин и наследуются аутосом-но-доминантно. Они ведут к преждевременному половому развитию из-за неуправляемого синтеза тестостерона во внутриутробном и в препубертатном периодах. При некоторых из этих мутаций высок риск опухолей яичка.
Применение гонадолиберина и его аналогов [ править | править код ]
В табл. 56.3 перечислены синтетические аналоги гонадолиберина, применяемые в клинике. Синтетический гонадолиберин называется гонадорелином. Замена аминокислотного остатка в положении 6 защищает аналоги гонадолиберина от протеолиза, а замена С-концевого остатка повышает сродство к рецептору. Такие аналоги обладают большей активностью и более длительным действием по сравнению с нативным гонадолиберином, Т1/2 которого составляет всего 2—4 мин.
Антагонисты гонадолиберина, в отличие от его аналогов длительного действия, не вызывают кратковременного повышения уровней гонадотропных гормонов в сыворотке. Современные антагонисты гонадолиберина, по-видимому, не приводят к местному и системному выбросу гистамина и анафилакгоидным реакциям, что ограничивало применение первых препаратов этой группы. Два антагониста гонадолиберина гаиреликс и цетрореликс применяют при искусственном оплодотворении для подавления выброса ЛГ во время стимуляции яичников. Ганиреликс доступен в США, а цетрореликс—только в Европе. Теоретически быстрое подавление выброса ЛГ дает возможность лучше контролировать стимуляцию яичников (см. ниже) и тем самым сокращает цикл искусственного оплодотворения. Однако практическую ценность этих препаратов при искусственном оплодотворении еще предстоит уточнить в клинических испытаниях.
Диагностическое применение [ править | править код ]
Один из препаратов гонадорелина (гонадорелина гидрохлорид) применяют для дифференциальной диагностики гипофизарного и гипоталамического поражения при вторичном гипогонадизме. Уровень ЛГ в сыворотке измеряют до введения гонадорелина в дозе 100 мкг п/к или в/в и в течение 2 ч (через 15,30,45,60 и 120 мин) после введения. Увеличение секреции ЛГ свидетельствует о наличии функционирующих гонадотропных клеток аденогипофиза. При длительном дефиците гонадолиберина чувствительность гонадотропных клеток к нему может снижаться, поэтому низкий уровень ЛГ при проведении пробы с гонадолиберином не обязательно говорит о поражении гипофиза. Пробу с гонадолиберином можно также использовать для дифференциальной диагностики истинного (связанного с секрецией гонадолиберина) и ложного преждевременного полового развития.
Лечение бесплодия [ править | править код ]
Другой препарат гонадорелина (гонадорелина ацетат) используют при нарушениях репродуктивной функции, связанных с дефицитом гонадолиберина. Препарат вводят в/в с помощью специального инфузионного насоса в импульсном режиме, имитирующем физиологическую секрецию, 2,5 мкг каждые 60—90 мин. Если овуляция не наступает, доза, вводимая за один импульс, может быть постепенно увеличена до 10 мкг. Принципы введения и дозы указаны в инструкции изготовителя. Гонадорелин реже, чем гонадотропные гормоны, вызывает многоплодную беременность. При лечении гона-дорелином не требуется столь тщательно контролировать уровень эстрогенов в сыворотке и проводить УЗИ яичников. Побочные реакции возникают редко, чаще всего развивается флебит в месте введения. При лечении гонадорелином у женщин восстанавливается физиологическая секреция половых гормонов, устанавливается менструальный цикл и происходит овуляция. Однако из-за технической сложности этот метод лечения применяют только в специализированных клиниках (Hayes et al., 1998).
При бесплодии у мужчин с помощью гонадорелина можно добиться роста яичек, нормальной секреции половых гормонов и сперматогенеза. Однако метод относительно дорог и требует постоянного ношения инфузионного насоса. К тому же гонадорелин не одобрен ФДА для лечения мужского бесплодия. Поэтому обычно предпочтение отдают гонадотропным гормонам.
Аналоги гонадолиберина длительного действия применяют также при индукций овуляции. Эти препараты подавляют предовуляторный выброс ЛГ и предотвращают лютеинизацию неовулирующего фолликула. Разработано несколько схем лечения, при которых длительно или краткосрочно вводят аналоги гонадолиберина совместно с гонадотропными гормонами, обеспечивающими созревание фолликула (см. ниже), а затем для индукции овуляции назначают ХГ (Lunenfeld, 1999).
Подавление секреции гонадотропных гормонов [ править | править код ]
Как уже говорилось, аналоги гонадолиберина длительного действия ведут к десенситизации рецепторов гонадолиберина, в результате чего секреция гонадотропных, а соответственно и половых, гормонов резко снижается. Такая «медикаментозная кастрация» оказалась очень удобной в тех случаях, когда нужно сократить выработку половых гормонов. Очевидное показание к подобному лечению — истинное преждевременное половое развитие у детей, при котором длительное введение аналогов гонадолиберина очень эффективно и почти не сопровождается побочными реакциями.
Аналоги гонадолиберина длительного действия используют для паллиативного лечения гормонально-зависимых опухолей (например, рака предстательной или молочной желез); поскольку в начале лечения эти препараты резко усиливают секрецию половых гормонов, одновременно назначают препараты, нарушающие синтез или блокирующие действие половых гормонов. Кроме того, аналоги гонадолиберина длительного действия используют при других гормонально-зависимых заболеваниях (эндометриозе, миоме матки и острой перемежающейся порфирии). Наконец, для медикаментозной кастрации при таких психических расстройствах, как педофилия, когда очень высок риск несоблюдения врачебных предписаний, особенно удобен гозерелин, который вводят в дозе 10,8 мг п/к 1 раз в 3 мес.
Аналоги гонадолиберина длительного действия в целом хорошо переносятся и вызывают вполне предсказуемые побочные эффекты, обусловленные нарушением синтеза половых гормонов: приливы, сухость влагалища, атрофический вагинит, снижение плотности костной ткани. В связи с этим при таких заболеваниях, как эндометриоз и миома матки, лечение обычно продолжают не более 6 мес или дополнительно назначают эстрогены для поддержания плотности костной ткани.
Диагностическое применение гонадотропных гормонов [ править | править код ]
Тест на беременность [ править | править код ]
В крови и моче беременных в больших количествах присутствует ХГ, поэтому в качестве теста на беременность можно использовать иммунохимическое выявление β-субъединицы ХГ. Качественное определение β-субъединицы ХГ в моче лежит в основе тестов на беременность для домашнего применения, продаваемых в США без рецепта. Эти тесты позволяют быстро выявить беременность уже через несколько дней после задержки менструации.
Количественное определение концентрации ХГ в плазме в клинических и научных целях проводят с помощью РИА. Обычно это делают для оценки прогрессирования беременности, а также при подозрении на внематочную беременность, пузырный занос или хориокарциному.
Определение времени овуляции [ править | править код ]
Овуляция происходит через 36 ч после начала выброса ЛГ и через 10—12 ч после достижения пика его концентрации. Поэтому по концентрации ЛГ в моче можно предсказать время овуляции. Для домашнего использования выпускают наборы, позволяющие при помощи специфических антител полуколичественно оценить уровень ЛГ в моче. Тест проводят каждые 12 или 24 ч начиная с 11 -го дня цикла (при 28-дневном цикле) и по увеличению уровня Л Г определяют предполагаемое время овуляции. Это дает возможность повысить вероятность зачатия путем правильного выбора времени для полового сношения.
Диагностика расстройств репродуктивной функции [ править | править код ]
Количественное измерение уровня ФСГ и ЛГ в плазме методом РИА (по уровню β-субъединиц) используют для диагностики некоторых нарушений репродуктивной функции. Низкие или неопределяемые уровни ФСГ и ЛГ свидетельствуют о вторичном гипогонадизме и о поражении гипофиза или гипоталамуса. При первичном гипогонадизме уровни этих гормонов, наоборот, высокие. При аменорее у женщин или задержке полового развития у мужчин и женщин определение уровня ФСГ и ЛГ позволяет отличить поражение половых желез от поражения гипоталамо-гипофизарной системы.
По уровню ФСГ на 3-й день менструального цикла можно судить о фертильности. Даже при нормальном менструальном цикле уровень ФСГ 15 МЕ/мл и более говорит о низкой фертильности, и успех искусственного оплодотворения при этом маловероятен (см. ниже).
Проба с ХГ используется у мужчин для оценки функции клеток Лейдига по степени стимуляции синтеза тестостерона. Эту пробу попользуют при подозрении на нарушение функции клеток Лейдига (например, при задержке полового развития). Уровень тестостерона в сыворотке определяют после нескольких инъекций ХГ. Сниженная секреция тестостерона говорит о патологии клеток Лейдига, а нормальная — о поражении гипоталамо-гипофизарной системы.
Лечебное применение гонадотропных гормонов [ править | править код ]
Изначально гонадотропные гормоны для клинического применения получали из человеческих гипофизов (трупный материал) и из мочи женщин. Препараты гипофиза сейчас не используют из-за риска передачи возбудителя болезни Крейтцфельдта—Якоба. Из мочи получают несколько препаратов. ХГ, который по действию аналогичен Л Г, получают из мочи беременных. Из мочи женщин в постменопаузе получают препарат менотропин, который содержит примерно одинаковые количества ЛГ и ФСГ, а также другие белки мочи. Поскольку менотропин относительно плохо очищен, во избежание аллергических реакций его вводят в/м. Другой препарат — урофоллитропин — представляет собой очищенный ФСГ, получаемый путем удаления ЛГ иммунологическими методами. Урофоллитропин сверхвысокой очистки получают при помощи моноклональных антител к ФСГ. Он очищен настолько, что его можно вводить п/к.
Методами генной инженерии получена линия клеток млекопитающих, синтезирующая а- и р-субъединицы ФСГ. Получающийся при этом рекомбинантный ФСГ близок по характеру гликозилирования к нативному ФСГ. Сегодня выпускается два препарата рекомбинантного ФСГ — фоллитропин а и фоллитропин Р; их углеводные структуры слегка различаются. Оба эти препарата вводят п/к, поскольку они намного чище препаратов, получаемых из мочи, и значительно лучше стандартизованы. Рекомбинантные препараты стоят намного дороже нативных, однако данных за то, что они эффективнее или реже вызывают такие побочные реакции, как синдром гиперстимуляции яичников, пока нет. Вероятно, в будущем методами генной инженерии удастся получить аналоги гонадотропных гормонов более длительного действия и с более высокой активностью.
Женское бесплодие [ править | править код ]
Бесплодием страдают около 10% супружеских пар детородного возраста. Для лечения бесплодия все шире применяют гонадотропные гормоны (Vollenhoven and Healy, 1998); часто их используют при искусственном оплодотворении. Хотя основным показанием к их назначению служит хроническая ановуляция в результате вторичного гипогонадизма (группа 1 по классификации ВОЗ), гонадотропные гормоны используют и для индукции овуляции при синдроме поликистозных яичников (группа II по классификации ВОЗ) в том случае, когда кломифен неэффективен (гл. 58). Кроме того, гонадотропные гормоны применяют при бесплодии на фоне нормальной овуляции, хотя в этих случаях сначала пробуют лечение кломифеном. Назначать гонадотропные гормоны должны врачи с достаточным опытом лечения бесплодия и эндокринных расстройств.
При хронической ановуляции назначение одного ФСГ в большинстве случаев вызывает овуляцию. Обычно ФСГ назначают в дозе 75 МЕ/сут в течение первых 6—7 дней цикла, после чего при помощи влагалищного УЗИ оценивают число и размер созревающих фолликулов. УЗИ обычно проводят каждые 2—3 сут. Созревание фолликула считается адекватным, если обнаружен фолликул диаметром 18 мм. Если обнаружено три и более фолликула диаметром более 16 мм, ФСГ отменяют из-за опасности синдрома гиперстимуляции яичников (см. ниже) и применяют барьерные методы контрацепции для предотвращения многоплодной беременности. Определяют также концентрацию эстрадиола, которая должна находиться в диапазоне 500—1500 пг/мл. Более низкие значения указывают на недостаточную стимуляцию яичников, а более высокие — на опасность синдрома гиперстимуляции яичников. При недостаточной стимуляции яичников доза ФСГ может быть увеличена до 150 МЕ/сут.
Для завершения созревания фолликула и индукции овуляции на следующий день после отмены ФСГ назначают ХГ в дозе 5000—10 000 ME. При лечении гонадотропными гормонами в 10—20% случаев развивается многоплодная беременность, что связано с развитием нескольких третичных фолликулов и выходом нескольких яйцеклеток.
Гонадотропные гормоны используют при искусственном оплодотворении, в том числе при экстракорпоральном оплодотворении и микроинъекции сперматозоидов в цитоплазму яйцеклетки. С помощью ФСГ стимулируют развитие фолликулов, а для окончательного их созревания назначают ХГ, после чего зрелые яйцеклетки извлекают из третичных фолликулов хирургическим путем. Затем производят экстракорпоральное оплодотворение полученных яйцеклеток с помощью спермы или микроинъекции сперматозоидов в цитоплазму яйцеклетки. Эмбрионы переносят в полость матки или в маточную трубу. При искусственном оплодотворении риск многоплодной беременности зависит от числа перенесенных эмбрионов.
Помимо многоплодной беременности и ее возможных осложнений основным побочным эффектом гонадотропных гормонов является синдром гиперстимуляции яичников. Для этого синдрома характерно быстрое накопление жидкости в полости брюшины, плевральной полости и даже перикарде. Считается, что причина этого синдрома — выделение яичниками вещества, повышающего сосудистую проницаемость. Синдром гиперстимуляции яичников проявляется вздутием живота, болью в животе, тошнотой, рвотой, поносом, выраженным увеличением яичников, одышкой и олигурией. Синдром гиперстимуляции яичников может осложниться гиповолемией, водно-электролитными нарушениями, гемоперитонеумом, РДСВ, тромбоэмболиями и нарушением функции печени. При подозрении на развитие этого синдрома ХГ не назначают.
В некоторых исследованиях выдвигалось предположение, что гонадотропные гормоны увеличивают риск рака яичников, однако это осталось недоказанным. Важно отметить, что при стимуляции яичников ФСГ и менотропином не возрастает риск пороков развития у детей, рожденных из стимулированных яйцеклеток.
Мужское бесплодие [ править | править код ]
Лечение гонадотропными гормонами может быть эффективно, если причина бесплодия — их дефицит. Поскольку гонадотропные гормоны относительно дороги, а при длительном приеме может развиться резистентность к ним, обычно половое развитие стимулируют андрогенами, а гонадотропные гормоны применяют позже, для достижения собственно фертильности.
Лечение, как правило, начинают с введения ХГ в дозе 1000— 5000 ME в/м 3 раза в неделю до нормализации синтеза половых гормонов, о чем судят по клиническим признакам и уровню тестостерона в плазме. После этого дозу ХГ снижают до 2000 ME 2 раза в неделю и дополнительно вводят менотропин в дозе по 75—150 ME ЛГ и ФСГ 3 раза в неделю. Наиболее частое побочное действие гонадотропных гормонов — гинекомастия; она возникает почти у каждого третьего больного и, вероятно, связана с повышенной продукцией эстрогенов: Для созревания яичек требуется примерно 6 мес, а для установления полноценного сперматогенеза лечение приходится продолжать до 2 лет. После начала сперматогенеза или его возобновления (при вторичном гипогонадизме, возникшем после полового созревания) для продукции спермы достаточно поддерживающей терапии I ХГ. Как уже говорилось, все большую роль в лечении бесплодия, вероятно, будут играть рекомбинантные гонадотропные гормоны.
Крипторхизм [ править | править код ]
При крипторхизме одно или оба яичка не , опускаются в мошонку. У доношенных новорожденных мальчиков он встречается в 3% случаев, но с возрастом его распространенность заметно снижается. При крипторхизме нарушается сперматогенез и повышается риск герминогенных опухолей яичка. Поэтому считается, что низведение яичка в мошонку следует производить как 3 можно раньше, обычно в возрасте года и уж во всяком случае до 2 лет. Поскольку опущение яичка стимулируется андрогенами, в отсутствие анатомического препятствия можно использовать ХГ. Обычно назначают 6 инъекций ХГ по 500 МЕ/м2 в/м через день. При неэффективности такого лечения производят орхипексию.
Читайте также [ править | править код ]
Предупреждение [ править код ]

Эстрогены (эстрадиол)
Применение андрогенно-анаболических стероидов (ААС) связано с определенными проблемами, если не подходить к этому ответственно и обдуманно. Все проблемы связаны с повышением гормонального фона у тех, кто их принимает, что требует регулярного и точного контроля. Как правило, те, кто к данной проблеме относится без предостережения, получают от приема препаратов лишь одни разочарования и вред. В результате необдуманного приема ААС, атлеты не получают ожидаемых положительных результатов, а вот вред для своего здоровья им обеспечен. Становится очевидным, что проблемы напрямую связаны с нарушением равновесия половых гормонов, таких, как мужской гормон тестостерон и женский – эстрадиол, прогестерон и пролактин. В данном случае, речь пойдет о женском гормоне эстрадиоле у мужчин.
Эстроген – это женский половой гормон, который является прямой противоположностью мужского гормона тестостерона. Он вырабатывается организмом мужчины, но в незначительных количествах, что никак не влияет на поведение мужчины и его жизнедеятельность. Превышение в организме мужчины женского гормона приводит к серьезным нарушениям функций организма, а также к изменению внешнего вида мужчины. К сожалению, его недостаточное количество в крови приводит к не менее серьезным последствиям. В связи с этим, мужчина обязательно должен контролировать свой гормональный фон, тем более, если использует определенные препараты в своей жизни.
При нарушении равновесия половых гормонов, когда женские гормоны начинают преобладать, в мужском организме происходят серьезные перестройки. Подобный дисбаланс часто наблюдается в процессе полового созревания мальчиков, который происходит в 11-15 лет, и характеризуется наличием в крови эстрадиола, причем в больших количествах. В результате наблюдаются отклонения в физиологическом развитии мальчика, что может привести к неполноценному росту половых органов, ожирению по женскому типу, гинекомастии. К тому же, избыток женских половых гормонов может привести к тому, что голос мальчика так и останется детским, а его поведение никак не назовешь мужским. Подобные изменения могут носить генетический характер, происходить из-за не правильного питания, а также вследствие различных заболеваний.
К сожалению, избыток эстрогена одинаково действует как на организм мальчика, так и на организм взрослого мужчины (атлета). Избыток женских половых гормонов может возникнуть не только в результате приема препаратов ААС, но и в результате нездорового питания и неправильного образа жизни. Особое внимание следует уделить приему алкоголя, а особенно пива.
Причины повышения уровня эстрадиола у мужчин
Существует много причин, на основе которых возможно увеличение уровня эстрогенов у мужчин. Например:
- Проблема со щитовидной железой.
- Проблемы с яичниками (опухоли или кисты).
- Лишний вес (ожирение).
- Заболевание печени.
- Заболевание почек.
- Употребление алкоголя (тем более пива).
- Гинекомастия.
- Прием анаболических стероидов.
В случае обнаружения повышенного уровня эстрадиола, в первую очередь следует сконцентрироваться на определении причин и лишь затем избавляться от последствий.
Для этого лучше обратиться к врачу и сделать анализы на гормоны щитовидной железы, сделать УЗИ, МРТ щитовидной железы, печени и почек.
Одной из основных причин повышения эстрадиола у мужчин – это излишки жировой ткани. Все дело в том, что жировая ткань принимает участие в работе эндокринной системы, что в свою очередь, связано с выделением гормонов. Зависимость такова, что чем выше уровень жировой ткани в организме мужчины, тем больше в крови эстрадиола.
Причем, проблемы на этом не заканчиваются: очень важно определиться с причинами ожирения. Если причинами служат чрезмерное питание и малоподвижный образ жизни, то проблема решается довольно просто: достаточно заняться спортом и умеренно питаться. Если ожирение – это процесс, который появился из «ниоткуда», то следует немедленно провести анализ состояния организма. Скорее всего, в организме произошел сбой в работе.
Понижение уровня эстрадиола на курсе стероидов
Организм человека всегда работает так, чтобы баланс не нарушался. Когда в крови появляется избыток мужского полового гормона, организм принимает меры для того, чтобы уровень гормона вернулся к первоначальному значению. Происходит это за счет ароматизации, когда избыток тестостерона превращается в эстрадиол. Довольно часто этот процесс происходит весьма активно и избыток эстрадиола у мужчин принимает серьезные показатели. Причем, данный процесс зависит от некоторых факторов, которые влияют на процесс ароматизации. К ним можно отнести избыток жира в организме, активность фермента ароматазы и другие.
На этапе приема стероидов борьба с повышенным уровнем эстрогена осуществляется с помощью ингибиторов ароматазы. Подобные вещества существенно подавляют механизм ароматизации, что снижает уровень эстрогена у мужчин. К таким препаратам относятся: анастрозол, летрозол, аримидекс, селана и т.д.
Но перед тем, как прибегнуть к приему подобных препаратов желательно определиться с уровнем эстрадиола, что даст возможность впоследствии контролировать процесс снижения его уровня в крови.
Как принимать ингибитор ароматазы на курсе стероидов
Принимаются ингибиторы ароматазы по 1 таблетке (0,5 мг) 2-3 раза в неделю. После курса приема в 7-10 дней следует сдать кровь на анализ. В случае понижения уровня эстрадиола до нормальной величины, то дозировка препарата снижается вдвое (0,5 таблетки 2 раза в неделю). Если уровень эстрадиола все еще выше нормы, то прием препарата продолжают по первоначальной дозировке.
В таком случае удастся поддержать уровень гормонов в норме при приеме ААС. Проблема сводится не только к проявлениям гинекомастии, но и к проблемам гипофиза – гипоталамуса – яичек. Если вовремя не обнаружить данную проблему, то восстановление займет гораздо больше времени.
Необходимо сразу заметить, что принимать препараты ААС не рекомендуется, если имеется значительная жировая прослойка. Идеальный вариант для начала приема фармакологии – это уровень жира, достигающий 12% и не больше. При таком уровне жира в организме достаточно легко поддерживать гормональный фон. К тому же, занятия спортом дадут наивысший результат.
Ну и самое главное! Слишком низкий уровень эстрадиола таит в себе не менее угрожающие опасности для мужчины – это снижение потенции, падение либидо, повышение хрупкости суставов, снижение иммунитета и другие последствия.
Задача заключается в том, чтобы поддерживать свой гормональный фон на природном уровне, что достигается только за счет обдуманных решений. Никогда не следует экономить на своем здоровье, а тем более относиться к нему с пренебрежением.
Послекрурсовая терапия после длительных курсов
Послекурсвая терапия после длительных курсов существенно отличается от «классического» ПКТ. Для начала следует разъяснить, что такое длительный курс. Длительный курс – курс, который длиться более 10 недель. Люди, занимающиеся профессионально спортом длительно готовятся к соревнованиям, что обуславливает такие длительные курсы, как 16-20 недель, иногда и больше. Обычная длинна курсов для людей, которые не являются профессиональными спортсменами, должна быть порядка 6-10 недель. За данное время, 6-10 недель, нет сильной атрофии тестикул, поэтому ПКТ относительно короткое и без таких препаратов как хорионический гонадотропин человека (ХГЧ) и менопаузный гонадотропин (МГ). При длительных курсах необходимо использовать ХГЧ на курсе, для поддержания секреции собственного тестостерона, что препятствует атрофии тестикул, также необходимо использовать ХГЧ после курса, как начало ПКТ, для стимуляции тесткул на синтез тестостерона, а только потом переходить к приему антиэстрогенов (кломифена цитрата или тамоксифена цитрата, торемифен).
2. Анализы и действия на курсе.
На курсе постоянно следует сдавать ряд анализов, для отслеживания состояния гормональной системы. Даже если у человека не возникает побочных эффектов, отслеживания гормонов важно для мониторинга здоровья.
На самом курсе следует отслеживать два основные гормоны:
Повышение эстрадиола или пролактина может способствовать сильной задержке жидкости, что в свою очередь может негативно отражаться как на аратериальном давлении, так и на состоянии сердечнососудистой системы. Отдельный побочный эффект – гинекомастия, увеличение железистой ткани в области сосков или отложение жира по женскому типу в области сосков. Не ведет к серьезным нарушениям здоровья, но эстетически неприятная вещь, которую желательно избегать.
Поэтому при повышении данных гормонов следует использовать два препарата:
Анастрозол – ингибитор ароматазы, снижает уровень эстрадиола в крови.
Каберголин – подавляет секрецию пролактина, снижает уровень пролактина в крови.
Понижение эстрадиола или пролактина ниже референсных значений также не желательно. Пролактин участвует в иммунных реакциях. Эстрадиол задерживает жидкость в организме, участвует в росте мышц вместе с тестостероном, влияет на уровень холестерина, способствуя повышению уровня ЛПВП, участвует в регуляции нервной системы. Поэтому при сильном понижении эстрадиола или пролактина следует корректировать дозу Анастрозола или Каберголина.
Хорионический гонадотропин на курсе.
На длительном курсе начинается атрофия тестикул, из-за того, что организм перестает выделять тестостерон, который попадет извне. Сильная атрофия тестикул ведет к сложному и длительному ПКТ. Поэтому для «облегчения» ПКТ следует предпринять ряд мер, и основная из них – стимуляция секреции тестикул ХГЧ.
ХГЧ обладает функциями лютеинизирующего (ЛГ) и фолликулостимулирующего гормонов гормона (ФСГ), но все же в большей степени обладает именно функциями ЛГ. ЛГ стимулирует клетки Лейдинга, которые вырабатывают тестостерон, в свою очередь ФСГ стимулирует клетки Сертоле, отвечающие за сперматогенез. Поэтому прием ХГЧ на курсе способен держать тесткикулы в «рабочем состоянии» и препятствовать их атрофии.
Продолжительность и дозировки ХГЧ.
ХГЧ на курсе следует колоть не постоянно, а с небольшими перерывами, порядка 3 недель колоть, и 3-4 недель отдыха. Поддерживающая доза ХГЧ 500 ЕД раз в 2-3 дня на протяжении 3 недель, после чего следует сделать перерыв для предотвращения десенситизации (потери чувствительности рецепторов клеток к препарату).
ХГЧ в конце курса идет в большей дозировке, от 1000 ЕД до 2500 ЕД черед день на протяжении 20 дней (10 уколов). Более длительный прием ведет к десенситизации.
Послекурсовая терапия после длительных курсов может занимать длительное время и проходить в несколько этапов.
Этап первый – выход с курса.
Анализы перед началом первого этапа:
При повышении или понижение данных гормонов следует скорректировать дозу ингибиторов ароматазы (анастрозола) и дофаминометиков (каберголина), чтобы эстрадиол и пролактин находились в референсных значениях, желательно на средине или ниже средины, в худшем случае – на высшей границе нормы, но в коем случае не выше референсных значений.
На первом этапе следует правильно выйти с курса анаболических стероидов. Следует понимать, что все стероиды имеют различные эфиры, тем самым могут длительно находиться в месте депо и попадать в кровь. Послекурсовую терапия следует начинать только тогда, когда анаболические стероиды полностью выйдут из крови и пройдут минимум 3 этапа полувыведения. Три этапа полувыведения не выведят полностью весь препарат с крови, но концентрация стероидов упадет до того уровня, при котором уже можно начинать полноценное восстановление.
К примеру: период полувыведения тестостерона пропионата – двое суток, значит после 6 суток можно начинать послекурсовую терапию.
Именно по этой причине следует заканчивать курс на более коротких эфирах, пропионате или финилпропионате, чтобы время вывидения препарата занимало 6-10 дней, а не затягивалось на 30-40 дней. Частая ошибка, когда люди начинают ПТК, пока в крови еще есть экзогенный стероид, который не позволяет запускаться секреции собственного тестостерона.
Этап второй – стимуляция секреции тестостерона ХГЧ.
Второй этап начинается после первого, возможно даже чтобы второй этап немного накладывался на первый, это значит, что можно колоть ХГЧ пока идет второй или третий этап полувыведения препаратов. Но самое главное, чтобы прием ХГЧ закончился позже или одновременно с 3-4 этапом полураспада стероидов. Чтобы не было ситуации, когда прием ХГЧ окончен, а в крови еще достаточно высокий уровень экзогенного тестостерона, в таком случае прием ХГЧ был бесполезен, с точки зрения начала ПКТ. Дозировки описаны в прошлой главе.
Анализы в конце второго этапа:
Эстрадиол и пролактин уже должны находиться в референсных значениях, после коррекции препаратов перед началом первого этапа, после это следует прекращать прием анастрозола и каберголина.
Этап третий – стимуляция секреции тестостерона антиэстрогенами.
На данном этапе начинается прием двух антиэстроегов: кломфен цитрат и торемифен. Данные два препарата похожи по своему действию, но все же имеют некоторые отличия, на практике и в исследованиях (ссылка внизу страницы) было доказано, что вместе они работают лучше, особенно при восстановлении от длительных курсов (на коротком курсе можно использовать и один антиэстроген). Длительность приема данных препаратов порядка 40-50 дней. Далее следует оканчивать ПКТ, а при необходимости продолжать (про это позже).
- Кломифен цитрат – 20 дней по 100 мг, 15 дней по 50 мг и 10 дней по 25 мг.
- Торемифен – 25 дней по 40 мг, 20 дней по 20 мг.
Анализы в конце второго этапа:
При хороших анализах ПКТ окончена.
Этап четвертый – продолжение ПКТ при плохих анализах.
Если после длительного курса ПКТ закончиться так быстро – это хорошо, но часто бывает, что ПКТ следует продолжать. И бывают разные ситуации по гормонам, сейчас подробно их разберем и разберем, что делать в той или иной ситуации.
Ситуация первая – Тестостерон низкий, ЛГ и ФСГ низкое.
В данном случае следует полностью повторять послекурсовую терапию. Это значит, что угнетение оси Гипоталамус-Гипофиз-Яички (ГГЯ) было очень сильное, и поэтому следует провести ПКТ с самого начала, начиная с этапа 2 – курса ХГЧ. После приема ХГЧ следует приступить к приме антиэстрогенов.
От автора: Тут рекомендовать дозы я уже не могу, так как нужно смотреть реальные анализы конкретного человека, если ЛГ и ФСГ практически в нулях, нужны большие дозы атиэстрогенов и возможно даже два препарата. Если ЛГ и ФСГ уже ближе к референсной границе, возможно можно ограничится и одним атиэсрогеном, все очень индивидуально.
Отдельно следует добавить, если эстрадиол повышен – следует вместе с приемом ХГЧ добавить анастрозол. Даже если эстрадиол на высшей референсной границе, скорей всего он повыситься при приеме ХГЧ, и все равно нужно будет добавить анастрозол.
Ситуация вторая – Тестостерон низшая или средняя граница референсного значения, ЛГ и ФСГ – средина или высшая граница референсного значения.
В данном случае можно сказать, что ПКТ идет успешно, но из-за длительного угнетения оси ГГЯ необходимо длительное время для восстановления нормального уровня гормонов. В данном случае можно провести курс на ингибиторах ароматазы – анастрозоле. Есть ряд исследований показывающих эффективность повышения уровня тестостерона приемом ИА. Но, тут есть одна важная поправка, данная терапия ИА сработает только в том случае если ЛГ и ФСГ уже в нормальных референсных значениях, если они низкие – такая терапия не сработает.
Дозировки следует подбирать индивидуально в зависимости от того, какой уровень эстрадиола сейчас у человека и как уровень реагирует на прием анастрозола:
- Эстрадиол низкий – лучше отдохнуть и сделать терапию антиэстрогенами (кломифеном).
- Эстрадиол средина или высшая референсная граница – начать прием анастрозола и снизить уровень эстрадиола ниже средины или немного выше референсной границы.
Продолжительность и дозы ХГЧ:
1. Effect of long term deprivation of luteinizing hormone on Leydig cell volume, Leydig cell number, and steroidogenic capacity of the rat testis. Keeney DS, et al. Endocrinology 1988; 123:2906–2915.
2. Coviello A. D. et al. Low-dose human chorionic gonadotropin maintains intratesticular testosterone in normal men with testosterone-induced gonadotropin suppression //Journal of Clinical Endocrinology & Metabolism. – 2005. – Т. 90. – №. 5. – С. 2595-2602.
Источник статьи: http://mupvirc.ru/gormony/fsg-gormon-v-bodibildinge/