Все о гормонах: какие бывают, как работают, как их используют в медицине?
Андрей Смирнов СПИД.ЦЕНТР
Наши тела состоят из миллионов клеток, и для слаженной работы им постоянно нужно обмениваться информацией, чтобы координировать работу разных органов. Для этого у нас есть два принципиально разных канала передачи информации: нервный (с помощью нервных импульсов) и гуморальный — с помощью гормонов и некоторых других веществ. «СПИД.ЦЕНТР» публикует подробный разбор устройства гормонов и их использования в лечении.
Зачем нужны гормоны? Какую роль они играют в организме?
Наши тела состоят из миллионов клеток, и для слаженной работы им постоянно нужно обмениваться информацией, чтобы координировать работу разных органов. Для этого у нас есть два принципиально разных канала передачи информации: нервный (с помощью нервных импульсов) и гуморальный — с помощью гормонов и некоторых других веществ.
Что вы делаете, если нужно сообщить человеку информацию, но он находится на другом конце города? Проще всего позвонить или написать сообщение. Для похожих целей в нашем организме используется нервная система — когда мы хотим, например, поднять руку, мозг «звонит» определенным мышечным волокнам через «телефонные провода» — нервы — и отдает соответствующую команду. Но как быть, если нужно передать какое-то сообщение сразу всем жителям города? Звонить каждому — слишком долго. Для этого у нашего организма есть свои СМИ — их функцию выполняют гормоны.
Название гуморального пути передачи информации происходит от латинского слова humor — «жидкость», так как в этом случае регулирующее вещество (гормон) вырабатывается одними клетками и попадает в жидкие среды организма (кровь, лимфу, межтканевую жидкость). Когда он по ним распространяется, то оказывает влияние на работу других клеток (клеток-мишеней).
Гуморальный путь регуляции эволюционно гораздо более древний, чем нервный. Еще в первых многоклеточных организмах клетки научились общаться между собой с помощью специальных веществ задолго до возникновения прообраза нервной системы.
Чем отличается нервная регуляция от гормональной?
Нервная регуляция работает гораздо быстрее — импульс по нервным волокнам передается за доли секунды. А между тем, как гормон выделится, попадет в кровь и доберется до клетки-мишени, могут проходить десятки секунд. При этом гормоны действуют на мишени гораздо дольше, до тех пор, пока будут оставаться в крови. Это могут быть минуты, часы или даже дни.
К тому же нервная регуляция узконаправленная — нервный импульс передается только определенным группам клеток, связанным нервным окончанием. А когда гормон выделился в кровь, он может влиять на любую клетку с подходящим рецептором.
Поэтому, когда информацию нужно передавать быстро и точно, используется нервный путь, но если надо охватить сразу много клеток, то гуморальный. Например, во время ходьбы мозгу нужно очень быстро и точно напрягать и расслаблять десятки разных мышц, причем каждую их них — в строго определенный момент времени. Для этого отлично подходят нервные импульсы. Но чтобы отрегулировать уровень глюкозы в крови, нужно сообщить сразу всем клеткам организма, с какой скоростью они эту глюкозу могут из крови поглощать, и это гораздо удобнее сделать с помощью гормона.
В нашем организме оба пути регуляции объединены в общую систему нейрогуморальной регуляции и работают синхронно под контролем центральной нервной системы, гипоталамуса и гипофиза.
Чем гормоны отличаются друг от друга?
С точки зрения химической природы гормоны очень сильно различаются — они могут быть производными аминокислот (тироксин, адреналин), стероидами (кортизол, половые гормоны), полипептидами и белками (окситоцин, инсулин). При этом у всех гормонов есть общие свойства.
Гормоны секретируются специализированными железами и влияют на работу других органов и клеток за пределами самой железы.
Гормоны влияют на работу органов и клеток в очень маленьких концентрациях.
Гормоны влияют на клетки, связываясь с рецепторами — специальными белками на поверхности клеток. Если у клетки нет рецептора для соответствующего гормона, она никак не отреагирует на этот гормон.
Гормоны действуют через изменение скорости синтеза ферментов в клетках или через изменение скорости ферментативных реакций в клетках, но при этом сами не являются ферментами.
Как правило, у гормонов много различных физиологических эффектов и они по-разному влияют на органы и ткани.
То или иное вещество может не всегда выступать как гормон. Например, норадреналин — это гормон надпочечников, он влияет на тонус сосудов, работу сердца и других органов. В то же время он выделяется в синапсах и участвует в передаче сигналов между нейронами — в этом случае он уже играет роль нейромедиатора, а не гормона.
Где вырабатываются гормоны?
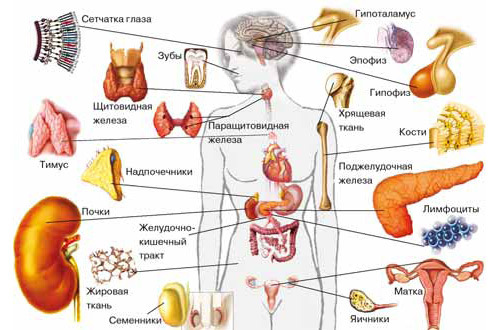
Большинство из них вырабатываются в специальных органах — железах внутренней секреции, или эндокринных железах. Основные из них:
Работа эндокринных желез регулируется гипоталамусом и гипофизом. В общем виде это выглядит так: гипоталамус под влиянием нервных импульсов выделяет специальные вещества — рилизинг-факторы. Они стимулируют выработку гормонов гипофиза (тропинов, или тропных гормонов), и уже под их влиянием другие железы начинают секретировать свои гормоны.
Важный элемент регуляции работы эндокринных желез — отрицательная обратная связь. Гипофиз постоянно контролирует концентрацию каждого гормона в крови, и когда какого-то гормона становится слишком много, он дает команду «горшочек, не вари» нужной железе.
Как связаны гормоны с биоритмами?
Уровень секреции гормонов в организме постоянно меняется. У одних гормонов он не ритмичен и зависит от внешних факторов, так, секрецию инсулина стимулирует прием пищи. Но все же секреция многих гормонов работает с четкой периодичностью — это называют циркадными ритмами. Их изучает отдельная наука — хронобиология.
Суточный ритм организма человека выглядит так: с наступлением темноты повышается секреция гормона сна — мелатонина. Это вещество синтезируется в эпифизе (шишковидной железе), способствует наступлению сна и выделяется всю ночь. Кстати мелатонин может с возрастом меньше синтезироваться — это одна из причин, почему пожилые люди чаще страдают бессонницей. А хронотипы сов и жаворонков появляются именно из-за разных по времени (разница в несколько часов) пиковых концентраций мелатонина и кортизола.
по теме
Лечение
Как устроен иммунитет: Объясняем по пунктам
Когда человек спит, также меньше выделяется гормонов надпочечников (гормонов стресса) и одновременно повышается секреция соматотропного гормона (СТГ) — он отвечает за стимуляцию роста различных тканей. Пик концентрации СТГ приходится на 2-3 часа ночи. Так что утверждение, что мы растем во сне, — научно доказанный факт.
Около 5-7 утра снова повышается выделение гормонов надпочечников, а с восходом солнца перестает синтезироваться мелатонин — все это помогает проснуться. Также на утренние часы приходится пик концентрации тестостерона, с чем связано возникновение утренней эрекции у мужчин.
Помимо суточных ритмов есть и более продолжительные циклы колебания уровня гормонов. Например, изменение уровня женских половых гормонов происходит с периодичностью примерно в 28 дней и регулирует течение менструального цикла. Причем концентрация гормонов существенно меняется на протяжении жизни. В подростковом возрасте гораздо больше синтезируется гормона роста, а в пожилом — существенно меньше вырабатывается половых гормонов.
Как гормоны используют в медицине?
Учитывая мощное и многогранное влияние гормонов на организм, многие из них широко применяются в медицинской практике. Есть несколько основных направлений их использования.
Первый — заместительная гормональная терапия (ЗГТ). Обычно именно ее имеют в виду, сообщая близким трагическим голосом: «Врач назначил мне гормоны» и «Я никогда с них не слезу», готовясь к каким-то ужасным побочным эффектам и необратимым изменениям в организме. На практике все оказывается гораздо прозаичнее: побочных эффектов почти нет или они быстро проходят, человек продолжает обычную жизнь, и ЗГТ на нее практически никак не влияет.
Эта терапия назначается, когда в организме не вырабатывается нужный гормон в необходимых количествах. Учитывая важную роль гормонов, своевременное назначение терапии позволяет избежать серьезных или даже необратимых проблем со здоровьем.
Как правило, гормональная терапия назначается пожизненно, так как в большинстве случаев причины подобных проблем современная медицина еще не научилась решать. И здесь важно не путать причину со следствием: невозможность «слезть с гормонов» связана не с влиянием самой ЗГТ, а с тем, что недостаточность собственной эндокринной функции никуда не исчезнет.
Возможно, страх перед ЗГТ связан с историческими причинами: первые препараты гормонов часто выделяли их желез животных (например, бычий или свиной инсулин), они содержали много примесей и действительно имели не самую хорошую переносимость. Сейчас для ЗГТ используют современные высокоочищенные препараты гормонов человека — они безопасны и эффективны.
В большинстве случаев при назначении гормональной терапии не нужна корректировка доз или отмена других препаратов (например, антиретровирусной терапии), так как ЗГТ имитирует естественную работу эндокринных желез. Но некоторые особенности течения основного заболевания все же нужно учитывать. Например, если лекарство содержит в качестве вспомогательных веществ глюкозу, мальтозу, сахар или другие углеводы, их количество нужно учитывать пациентам, получающим инсулин. Также следует учитывать влияние на активность печеночных ферментов некоторых АРВ-препаратов, например, ингибиторов протеазы. Если соответствующие печеночные ферменты участвуют в расщеплении назначенного гормонального препарата, может потребоваться коррекция дозы гормона — это проверяет и учитывает врач.
Могут ли гормонами лечить заболевания, не связанные с самими гормонами?
Да, это еще одно направление их использования. Например, адреналин повышает артериальное давление благодаря сокращению сосудов и усилению работы сердца. Поэтому его используют для лечения шоковых состояний, когда нужно быстро повысить артериальное давление. А у глюкокортикоидных гормонов мощное противовоспалительное действие, и они подавляют реакции иммунной системы, поэтому их очень широко используют при лечении аллергических заболеваний, бронхиальной астмы и других хронических воспалительных заболеваний.
Во многих случаях «природный» гормон помимо полезного эффекта для лечения заболевания обладает и нежелательными. У мужских половых гормонов есть мощное анаболическое действие — усиливают синтез белка и рост мышц. Это полезно при лечении людей с тяжелой степенью истощения (например, после сильных ожогов). Но в то же время они влияют на половую сферу, повышают агрессивность, могут приводить к чрезмерному увеличению предстательной железы.
Уменьшить ненужные «лишние» эффекты можно с помощью синтетических и полусинтетических аналогов. То есть подбираются вещества, близкие по химической структуре к природному гормону, но при этом у них «нужное» действие более выражено, а «лишние» минимизированы. Именно таким путем из природных мужских половых гормонов получили анаболики — они сильнее стимулируют синтез белка и меньше влияют на половую сферу, чем тестостерон. Сейчас синтетические аналоги гормонов применяют значительно чаще, чем сами природные гормоны.
Также в медицине используют антагонисты гормонов. Это вещества, которые связываются с рецептором природного гормона на поверхности клетки, но при этом характерного влияния не оказывают. Такие вещества часто используют для лечения заболеваний, связанных с избыточной секрецией гормона или когда вредны даже «нормальные» концентрации. Например, некоторые злокачественные опухоли активно растут под влиянием определенных гормонов, и чтобы остановить рост опухоли, нужно «выключить» действие гормона. Так, опухолям предстательной железы для роста часто требуется стимулирующее влияние тестостерона. Один из способов лечения — назначить бикалутамид. Этот препарат связывается с тестостероновыми рецепторами опухоли, блокирует влияние тестостерона и тормозит рост опухоли.
При назначении гормональных препаратов на фоне другой терапии, в том числе и АРВТ, требуется обязательная проверка совместимости препаратов, как и в случае совместного назначения любых других лекарственных средств.
Зачем трансгендерные люди пьют гормоны? И как это работает?
Половые гормоны влияют не только на развитие и функцию репродуктивной системы, но также и на развитие вторичных половых признаков, формируя «мужской» или «женский» внешний облик. Поэтому прием половых гормонов часто является важной частью трансгендерного перехода: такая терапия влияет на внешность гораздо сильнее хирургический операций.
Источник статьи: http://spid.center/ru/articles/2764/
Химическая природа и биологическое действие гормонов
АКТГ – адренокортикотропный гормон
ВНД – высшая нервная деятельность
ВМК – ванилилминдальная кислота
ГТГ – гонадотропные гормоны
ЛГ – лютеинизирующий гормон
ЛПВП – липопротеины высокой плотности
ЛПОНП – липопротеины очень низкой плотности
МСГ – меланоцитостимулирующий гормон
СТГ – соматотропный гормон
Т4 – тетраиодтиронин (тироксин)
Фн – фосфат неорганический
ФСГ – фолликулостимулирующий гормон
цАМФ – циклический аденозинмонофосфат
цГМФ – циклический гуанозинмонофосфат
ЦНС – центральная нервная система
Введение
Имеющаяся в учебниках обширная информация по теме «Биохимия гормонов» не позволяет студентам, впервые изучающим этот раздел, правильно сориентироваться в выборе главных моментов для понимания биологических эффектов и молекулярных механизмов действия гормонов на организм. Целью настоящего издания является предоставление студентам информации о биохимии гормонов в более четкой и ясной форме, что будет способствовать овладению учебной дисциплиной.
Материал пособия содержит описание общих закономерностей действия гормонов на клетку, а также обоснование и объяснение молекулярных механизмов влияния гормонов на организм в норме и при патологических состояниях.
Предлагаемый учебный материал поможет студентам глубже понять значимость регуляторных механизмов для согласованной работы органов и систем, а также научиться разбираться в сущности биохимических процессов, лежащих в основе метаболических нарушений при патологии эндокринной системы.
Гормоны
Из всех биологически активных соединений и субстратов, принимающих участие в регуляции биохимических процессов и функций, особая роль принадлежит гормонам.
Слово «гормон» происходит из греческого языка и означает «возбуждать», «приводить в движение».
Гормоны – это органические вещества, которые образуются в тканях одного типа (эндокринные железы, или железы внутренней секреции), поступают в кровь, переносятся по кровяному руслу в ткани другого типа (ткани-мишени), где оказывают своё биологическое действие (т. е. регулируют обмен веществ, поведение и физиологические функции организма, а также рост, деление и дифференцировку клеток).
Классификация гормонов
По химической природе гормоны делятся на следующие группы:
1. пептидные – гормоны гипоталамуса, гипофиза, инсулин, глюкагон, гормоны паращитовидных желез;
2. производные аминокислот – адреналин, тироксин;
3. стероидные – глюкокортикоиды, минералокортикоиды, мужские и женские половые гормоны;
4. эйкозаноиды – гормоноподобные вещества, которые оказывают местное действие; они являются производными арахидоновой кислоты (полиненасыщенная жирная кислота).
По месту образования гормоны делятся на гормоны гипоталамуса, гипофиза, щитовидной железы, паращитовидных желёз, надпочечников (коркового и мозгового вещества), женские половые гормоны, мужские половые гормоны, местные или тканевые гормоны.
По действию на биохимические процессы и функции гормоны делятся на:
1. гормоны, регулирующие обмен веществ (инсулин, глюкагон, адреналин, кортизол);
2. гормоны, регулирующие обмен кальция и фосфора (паратиреоидный гормон, кальцитонин, кальцитриол);
3. гормоны, регулирующие водно-солевой обмен (альдостерон, вазопрессин);
4. гормоны, регулирующие репродуктивную функцию (женские и мужские половые гормоны);
5. гормоны, регулирующие функции эндокринных желёз (адренокортикотропный гормон, тиреотропный гормон, лютеинизирующий гормон, фолликулостимулирующий гормон, соматотропный гормон);
6. гормоны стресса (адреналин, глюкокортикоиды и др.);
7. гормоны, влияющие на ВНД (память, внимание, мышление, поведение, настроение): глюкокортикоиды, паратиреоидный гормон, тироксин, адренокортикотропный гормон)
Свойства гормонов
Высокая биологическая активность. Концентрация гормонов в крови очень мала, но их действие сильно выражено, поэтому даже небольшое увеличение или уменьшение уровня гормона в крови вызывает различные, часто значительные, отклонения в обмене веществ и функционировании органов и может привести к патологии.
Короткое время жизни, обычно от нескольких минут до получаса, после чего гормон инактивируется или разрушается. Но с разрушением гормона его действие не прекращается, а может продолжаться в течение часов и даже суток.
Дистантность действия. Гормоны вырабатываются в одних органах (эндокринных железах), а действуют в других (тканях- мишенях).
Высокая специфичность действия. Гормон оказывает своё действие только после связывания с рецептором. Рецептор – это сложный белок-гликопротеин, состоящий из белковой и углеводной частей. Гормон связывается именно с углеводной частью рецептора. Причём строение углеводной части имеет уникальную химическую структуру и соответствует пространственному строению гормона. Поэтому гормон безошибочно, точно, специфично связывается только со своим рецептором, несмотря на малую концентрацию гормона в крови.
Не все ткани одинаково реагируют на действие гормона. Высокой чувствительностью к гормону обладают те ткани, в которых имеются рецепторы к данному гормону. В таких тканях гормон вызывает наиболее выраженные сдвиги в обмене веществ и функциях. Если рецепторы к гормону есть во многих, или почти во всех тканях, то такой гормон оказывает общее действие (тироксин, глюкокортикоиды, соматотропный гормон, инсулин). Если рецепторы к гормону присутствуют в весьма ограниченном числе тканей, то такой гормон обладает избирательным действием. Ткани, в которых имеются рецепторы к данному гормону, называются ткани-мишени. В тканях-мишенях гормоны могут воздействовать на генетический аппарат, мембраны, ферменты.
Типы биологического действия гормонов
1. Метаболическое – действие гормона на организм проявляется регуляцией обмена веществ (например, инсулин, глюкокортикоиды, глюкагон).
2. Морфогенетическое – гормон действует на рост, деление и дифференцировку клеток в онтогенезе (например, соматотропный гормон, половые гормоны, тироксин).
3. Кинетическое или пусковое – гормоны способны запускать функции (например, пролактин – лактацию, половые гормоны – функцию половых желёз).
4. Корригирующее. Гормонам принадлежит важнейшая роль в адаптации человека к различным факторам внешней среды. Гормоны изменяют обмен веществ, поведение и функции органов так, чтобы приспособить организм к изменившимся условиям существования, т.е. осуществляют метаболическую, поведенческую и функциональную адаптацию, тем самым поддерживают постоянство внутренней среды организма.
Механизм действия пептидных гормонов и адреналина
Рецепторы к этим гормонам находятся на наружной поверхности клеточной мембраны, и гормон внутрь клетки не проникает. Действие гормона в клетку передается при помощи так называемых вторых посредников, к которым относятся циклический АМФ (цАМФ), циклический ГМФ (цГМФ), кальций, инозитолтрифосфат, диацилглицерол (диглицерид) и некоторые другие. В системе передачи регуляторного сигнала они называются вторыми посредниками, потому что первым посредником является сам гормон.
Каждый из вторых посредников активирует специфическую протеинкиназу. Протеинкиназы фосфорилируют ферменты, и это изменяет активность ферментов.
Главным вторым посредником является цАМФ (рис. 1). Большинство гормонов действует через него. Другие посредники, действуя через свои протеинкиназы, могут изменять содержание цАМФ в клетке путём повышения или снижения активности ферментов, синтезирующих или разрушающих цАМФ.
Циклический АМФ образуется в клетке из АТФ под действием аденилатциклазной системы (рис. 2). В состав аденилатциклазной системы входят: рецептор, G-белок и фермент аденилатциклаза. G- белок называется так потому, что он способен связывать гуаниловые нуклеотиды (ГТФ или ГДФ). Существует 2 разновидности G-белка: Gs – стимулирует аденилатциклазу и увеличивает образование цАМФ и Gi – ингибирует аденилатциклазу и уменьшает образование цАМФ.
Белки Gs и Gi оказывают своё активирующее или ингибирующее действие только когда находятся в! активном состоянии. G-белок активен, когда он связан с ГТФ, и наоборот, связанный с ГДФ, G- белок неактивен.
Пока гормон не действует на клетку, аденилатциклазная система неактивна; все её компоненты разобщены и с G-белком связан ГДФ. Однако после связывания гормона с рецептором происходит последовательное изменение конформации всех компонентов аденилатциклазной системы, G-белок обменивает ГДФ на ГТФ, переходит в активное состояние и активирует аденилатциклазу, которая из АТФ синтезирует цАМФ. Циклический АМФ, в свою очередь, активирует специфическую цАМФ-зависимую протеинкиназу (протеинкиназу А), которая фосфорилирует внутриклеточные ферменты, в результате чего изменяется активность ферментов.
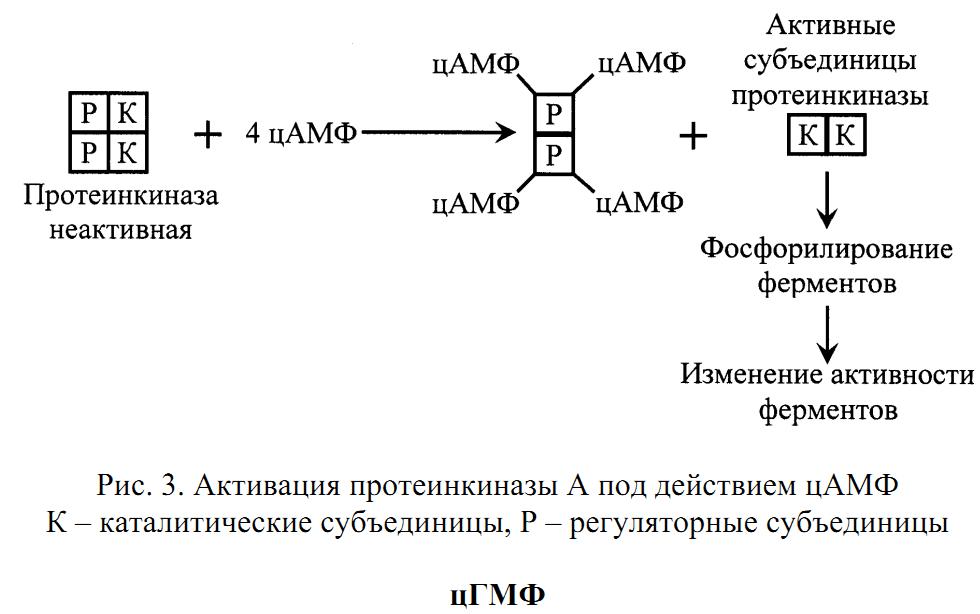
Протеинкиназа состоит из 4 субъединиц (тетрамер), две из которых являются регуляторными, а две – каталитическими (рис. 3. . В таком виде протеинкиназа неактивна. При связывании протеинкиназой 4 молекул цАМФ происходит отсоединение (диссоциация) каталитических субъединиц, которые фосфорилируют белки (ферменты), изменяя их активность.
Разрушается цАМФ фосфодиэстеразой.
Циклический ГМФ образуется из ГТФ под действием гуанилатциклазы по аналогии с синтезом цАМФ. Циклический ГМФ активирует специфическую цГМФ-зависимую протеинкиназу или протеинкиназу G, которая фосфорилирует ферменты, что сопровождается изменением их активности. Разрушается цГМФ, как и цАМФ, фосфодиэстеразой.
Кальций
Концентрация Са2+ во внеклеточной жидкости в 10 000 раз больше, чем в цитоплазме. Такая концентрация кальция оказалась бы потенциально летальной для клетки. Клетка борется с избытком Са2+ в цитоплазме путём откачивания его наружу с помощью Са2+- АТФазы, расположенной в плазматической мембране.
Под действием гормонального сигнала концентрация Са2+ в клетке возрастает в 10 и более раз за счет притока Са2+ из внеклеточной жидкости, а также выхода Са2+ из ЭПР и митохондрий. В клетке Са2+ связывается с белком кальмодулином и активирует специфическую Са2+-кальмодулин-зависимую протеинкиназу. В ГЛ 2+ ответ на гормональный сигнал и повышение концентрации Са в клетке специфическая протеинкиназа катализирует фосфорилирование множества внутриклеточных ферментов, регулируя, тем самым, их активность.
Инозитолтрифосфат и диглицерид
Эти вторые посредники являются производными фосфолипида мембран, фосфатидилинозитола. Указанный фосфолипид фосфорилируется в мембране под действием фермента фосфатидилинозитолкиназы при участии 2 молекул АТФ (рис. 4. .
Образующийся фосфатидилинозитолдифосфат расщепляется под действием специфического мембраносвязянного фермента фосфолипазы С, в результате чего образуются два вторых посредника: диглицерид (диацилглицерол, ДАГ) и инозитолтрифосфат (ИФ3.)
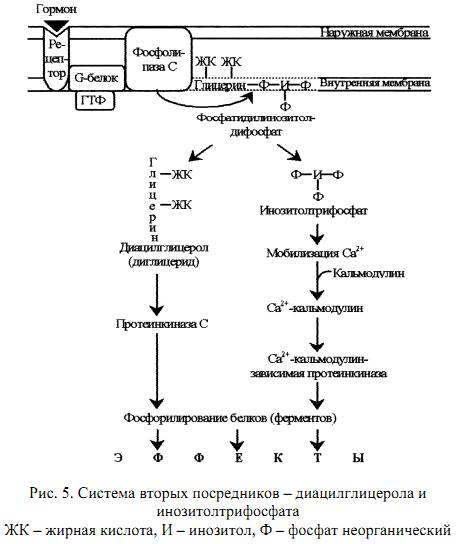
Биологические эффекты этих двух вторых посредников реализуются по-разному. ДАГ активирует Са2+-зависимую протеинкиназу С, которая катализирует фосфорилирование внутриклеточных ферментов, изменяя их активность. ИФ3 связывается со специфическим рецептором на ЭПР, способствуя выходу из него Са2+ в цитоплазму. Далее Са2+ связывается с кальмодулином и активирует Са2+-кальмодулин-зависимую протеинкиназу, которая катализирует фосфорилирование ферментов, изменяя их активность (рис. 5.)

Механизм действия стероидных гормонов и тироксина
Рецепторы к этим гормонам находятся внутри клетки, в цитоплазме. Гормон легко и быстро проникает через мембрану внутрь клетки, взаимодействует с рецептором с образованием гормон-рецепторного комплекса. Этот комплекс переносится в ядро, где связывается с ядерным хроматином в определенном участке ДНК. С этого участка ДНК начинается синтез специфических мРНК, которые затем выходят в цитоплазму и служат матрицей для синтеза ферментов или других белков, необходимых клетке и обеспечивающих ответ клетки на действие гормона (рис. 6. .
Таким образом, под действием пептидных гормонов и адреналина в клетке изменяется активность ферментов; стероидные гормоны и тироксин приводят к изменению количества ферментов.
Гормоны щитовидной железы
В щитовидной железе синтезируются тиреоидные гормоны – тироксин (Т4. и трииодтиронин (Т3. . Для синтеза этих гормонов необходим иод, который активно захватывается из крови клетками фолликулов щитовидной железы. Тироксин и трииодтиронин являются производными аминокислоты тирозина. Тироксин содержит в своей молекуле 4 атома иода, в состав трииодтиронина входит 3 атома иода.
В клетках эпителия фолликулов щитовидной железы находится белок тиреоглобулин. Это гликопротеин, содержащий много остатков аминокислоты тирозина (около 3 % от массы белка). Синтез тиреоидных гормонов идет из тирозина и атомов иода именно в составе молекулы тиреоглобулина и включает 2 стадии. На апикальных мембранах клеток фолликулов сначала происходит иодирование тирозина с образованием моноиодтирозина (МИТ) и дииодтирозина (ДИТ). Следующим этапом является конденсация МИТ и ДИТ с образованием Т3 и Т4 (рис. 7. .
Такая иодированная молекула тиреоглобулина секретируется в просвет фолликула, в коллоид. Когда в щитовидную железу приходит сигнал в виде ТТГ (тиреотропного гормона), клетки фолликула захватывают капельки коллоида вместе с тиреоглобулином, ферменты лизосом протеазы гидролизуют белок до аминокислот, и готовые Т3 и Т4 поступают в кровь.
В крови тиреоидные гормоны связываются с белком- переносчиком и в таком виде транспортируются в ткани-мишени. Концентрация Т4 в крови в 10 раз больше, чем Т3, поэтому Т4 называют главной формой тиреоидных гормонов в крови. Но Т3 в 10 раз активнее, чем Т4.
Ткани-мишени для тиреоидных гормонов – это все ткани, кроме селезёнки и семенников.
В тканях-мишенях тиреоидные гормоны освобождаются от белка и поступают в клетку. В клетках 90 % Т4 теряет 1 атом иода и превращается в Т3. Таким образом, главной внутриклеточной формой гормона является Т3.
Действие тиреоидных гормонов на организм зависит от концентрации этих гормонов в крови: в физиологических дозах они оказывают анаболическое действие, в больших дозах – катаболическое.
Действие физиологических (нормальных) концентраций Т4
Главное действие физиологических концентраций тиреоидных гормонов направлено на синтез белка и на энергетический обмен.
Действие Т4 на синтез белка. Через рецепторы цитоплазмы гормон действует на хроматин ядра, в результате чего увеличивается синтез нуклеиновых кислот (ДНК, мРНК) и белка. Наработка новых молекул белка ускоряет рост, деление и дифференцировку клеток, что особенно важно для растущего организма.
Тиреоидные гормоны абсолютно необходимы для структурного, биохимического и функционального созревания мозга. Считают, что в ЦНС клетки продолжают делиться в течение 1–1,5 лет после рождения. Поэтому если в этот период или еще до рождения возникает дефицит тиреоидных гормонов (гипотиреоз), это приводит к снижению синтеза белка во всем организме и, в частности, в мозговой ткани, нарушается процесс дифференцировки коры больших полушарий и мозжечка, и развивается умственная и физическая отсталость. Гипотиреоз у детей называется кретинизм. Чем раньше возникает дефицит тиреоидных гормонов, тем сильнее это сказывается на задержке развития ЦНС. Поэтому, чрезвычайно важна ранняя диагностика гипотиреоза, чтобы своевременно назначить адекватное лечение и избежать умственной отсталости.
Действие Т4 на энергетический обмен. Тиреоидные гормоны активируют энергетический обмен, т.е. расходование и синтез АТФ. Поскольку одновременно активируются 2 противоположно направленных процесса, между ними сохраняется равновесие. Внешне это проявляется увеличением потребления кислорода тканями и образованием тепла для поддержания нормальной температуры тела.
Молекулярный механизм действия тиреоидных гормонов на энергетический обмен заключается в следующем. Тиреоидные гормоны увеличивают расходование АТФ на энергозависимые процессы, в результате чего образуется АДФ. АДФ является активатором цепи тканевого дыхания (ЦТД), где из АДФ вновь образуется АТФ, которая снова расходуется на энергозависимые процессы.
Из всех энергозависимых процессов наиболее энергоёмким процессом является работа по поддержанию электрохимического градиента концентрации ионов Na+ и K+ по обеим сторонам клеточной мембраны. В процессе жизнедеятельности любая клетка, и нервная клетка в частности, может находиться в состоянии покоя и функционирования. В покое концентрация K+ в клетке больше, чем Na+, снаружи – наоборот. При функционировании клетки K+ выходит из неё, Na+ – входит в клетку.
Чтобы вернуть клетку в состояние покоя, надо выкачать из неё Na+ и ввести K+. Работу по восстановлению исходной концентрации ионов в клетке выполняет фермент ^+,К+-АТФаза. Процесс идет с затратой энергии АТФ, в результате чего образуется АДФ и Фн. №+Д+-АТФаза содержится в мембране всех клеток и является важнейшим ферментом для нормального функционирования нервной ткани. Важно отметить, что на работу ^^^-АТФазы расходуется большая часть энергии клетки (от 20 до 80 %, в среднем 50 % клеточных запасов АТФ).
Тиреоидные гормоны стимулируют №+Д+-АТФазу, тем самым увеличивая расщепление АТФ и образование АДФ и Фн в цитоплазме. АДФ затем переносится из цитоплазмы в митохондрию, где АДФ активирует ЦТД и, таким образом, повышает синтез АТФ, который используется при функционировании ^^^-АТФазы.
Таким образом, тиреоидные гормоны одновременно увеличивают использование АТФ и его образование, т. е. поддерживают энергетическое равновесие в клетке.
Сохранение энергетического равновесия очень важно для поддержания электрохимического градиента Na+ и K+ по обеим сторонам клеточной мембраны. Это является основой для нормального функционирования нервной ткани, т.е. для координации процессов возбуждения и торможения в мозге. Благодаря участию тиреоидных гормонов, процессы возбуждения и торможения в мозге скоординированы. При избытке или дефиците тиреоидных гормонов нарушается энергетическое равновесие, нарушаются электрохимические процессы в ЦНС, что сопровождается определёнными мозговыми симптомами.
Действие высоких (избыточных) концентраций Т4
При гипертиреозе (тиреотоксикоз, или Базедова болезнь) в организме образуется избыточное количество тироксина. Большие концентрации гормона действуют на митохондрии, которые являются «энергетическими станциями» клетки. В митохондриях находится ЦТД, т.е. цепь переносчиков, которая окисляет субстраты при помощи кислорода и в которой образуется энергия. В норме часть этой энергии запасается в виде АТФ, а часть идет на образование тепла для поддержания нормальной температуры тела. Образование АТФ в ЦТД называется окислительным фосфорилированием. Большие концентрации тиреоидных гормонов разобщают ЦТД и окислительное фосфорилирование. В результате ЦТД работает, субстраты окисляются, энергия в ЦТД образуется, но из-за разобщения ЦТД и окислительного фосфорилирования энергия не запасается в виде АТФ, а рассеивается в виде тепла. Поэтому одним из характерных признаков гипертиреоза является повышение температуры тела. Поскольку образование АТФ при этом заболевании снижается, то наблюдается сильная слабость, так как АТФ необходим для мышечного сокращения и поддержания тонуса мускулатуры. Дефицит АТФ в организме приводит к усиленному распаду белков, углеводов и жиров тела (катаболическое действие больших концентраций тироксина), что сопровождается резким общим похуданием.
Кроме перечисленных симптомов, при гипертиреозе наблюдаются: увеличение щитовидной железы (зоб), пучеглазие (экзофтальм), увеличение частоты сердечных сокращений (тахикардия), возбужденность, беспокойство, нервозность, плаксивость, бессонница, эмоциональная лабильность, потливость, кожа становится влажной и горячей.
Гипофункция щитовидной железы (гипотиреоз) у взрослых называется микседема. Развиваются слизеподобный отек тканей, ожирение, выпадение волос и зубов, апатия, сонливость, психическая инертность, снижение интереса и инициативы, гиперхолестеринемия, жировое перерождение печени, речь становится медленной и невнятной, мимика невыразительной, кожа – сухая, бледная и холодная, снижается температура тела.
Гипофункция щитовидной железы (гипотиреоз) у детей называется кретинизм (см. выше).
Особой формой гипотиреоза является эндемический зоб. Он возникает при недостаточном содержании йода в воде и пище. Компенсаторно разрастается ткань щитовидной железы, но при отсутствии иода это не приводит к увеличению выработки тиреоидных гормонов.
Гормоны паращитовидных желёз
В паращитовидных железах образуется паратиреоидный гормон (паратгормон) и кальцитонин. Однако основное количество кальцитонина вырабатывается в щитовидной железе.
Паратгормон – это гормон белковой природы, который повышает содержание кальция (Са ) и снижает концентрацию фосфата (Р) в крови. Действие паратгормона направлено на следующие ткани-мишени:
1. кости – гормон увеличивает выход Са и Р из кости в кровь; тормозит синтез коллагена в остеобластах, увеличивает разрушение минеральной и органической части кости остеокластами и остеоцитами;
2. кишечник – увеличивает всасывание Са2+ и Р из кишечника в кровь;
3. почки – увеличивает реабсорбцию Са2+ из мочи в кровь, но увеличивает выведение Р с мочой.
Патология
Гиперпаратиреоз – повышенное образование паратгормона, возникающее при опухоли паращитовидных желёз. Так как Са2+ усиленно выходит из кости, то наблюдаются самопроизвольные переломы вследствие рассасывания костной ткани. Повышение концентрации Са2+ в крови приводит:
1. к окостенению внутренних органов, обызвествлению ушибов, кровоподтёков;
2. к понижению нервно-мышечной возбудимости, что проявляется как атрофия и слабость мышц, а также депрессией, нарушением памяти и внимания.
Избыток паратгормона резко увеличивает секрецию гастрина, что, в свою очередь, приводит к повышению секреции HCl и пепсина в желудке, поэтому при избытке паратгормона могут развиться язвы желудка.
Гипопаратиреоз – может наблюдаться после операций на щитовидной железе, когда по ошибке были удалены и паращитовидные железы, либо возникает у детей при инфекциях дыхательных путей. Такое состояние сопровождается снижением концентрации Са2+ в крови, что приводит к повышению нервно- мышечной возбудимости. У взрослых наблюдаются конвульсии, судороги, что характеризуется как тетания. У детей может возникнуть спазмофилия, т.е. состояние, когда ребенок во время плача внезапно синеет из-за спазма дыхательных мышц.
Кальцитонин – понижает концентрацию и Са2+, и Р в крови. Оказывает влияние на те же ткани-мишени, что и паратгормон, однако действие кальцитонина, в основном, противоположно эффектам паратгормона. Однако, как и паратгормон, кальцитонин увеличивает выведение Р с мочой.
Гормоны поджелудочной железы
Инсулин – гормон белковой природы, синтезируется в р-клетках островков Лангерганса, запасается в секреторных гранулах в связи с цинком и выделяется в кровь в ответ на повышение концентрации глюкозы в крови.
По чувствительности к инсулину все ткани можно разделить на 3 группы:
1. Главные ткани-мишени или абсолютно зависимые от инсулина ткани. Они обладают максимальной чувствительностью к инсулину. К этой группе относятся жировая ткань и мышцы. Глюкоза не проникает в эти ткани и не утилизируется в них в отсутствие инсулина.
2. Абсолютно независимые от инсулина ткани. К ним относятся головной мозг, эритроциты, слизистая оболочка (эпителий) тонкого кишечника, мозговое вещество почек, семенники. В клетки этих тканей глюкоза проникает легко даже в отсутствие инсулина и является для них единственным энергетическим субстратом. Эти ткани (клетки) выполняют важнейшие функции организма: мозг – центральную регуляцию, эритроциты – транспорт кислорода, почки – экскрецию, тонкий кишечник – питание, семенники – воспроизводство (размножение). Причем мозг потребляет 50 % всей глюкозы организма, почки и эритроциты – ещё 20 %. Таким образом, для организма оказывается чрезвычайно важным то, что основной метаболический фонд глюкозы и жизненно важные функции оказываются независимыми от инсулина.
3. Относительно зависимые от инсулина ткани. Это все остальные ткани. По чувствительности к инсулину они занимают промежуточное положение между тканями 1-ой и 2-ой группы.
Действие инсулина на внутриклеточный метаболизм
1. Инсулин – единственный гормон, снижающий концентрацию глюкозы в крови. Такой эффект гормона обусловлен следующими механизмами:
• инсулин увеличивает проницаемость мембран для транспорта глюкозы из крови в клетки;
• инсулин активирует использование глюкозы по пути гликолиза (окислительный распад глюкозы) и на синтез гликогена;
• инсулин тормозит распад гликогена (гликогенолиз) и глюконеогенез (процесс образования глюкозы из аминокислот).
2. Инсулин является универсальным анаболическим гормоном. Он усиливает процессы синтеза нуклеиновых кислот, белка, жиров, гликогена и тормозит их распад. Кроме того, анаболическое действие инсулина проявляется в том, что он активирует процессы, дающие энергию для синтезов (гликолиз, цикл трикарбоновых кислот).
Патология
Сахарный диабет – заболевание, обусловленное недостатком инсулина в организме. Наблюдается повышенное содержание глюкозы в крови (гипергликемия), может появляться глюкоза в моче (глюкозурия), усиливается распад (катаболизм) белков, жира, гликогена, тормозится их синтез, активируется глюконеогенез и резко снижается активность гликолиза. В крови и моче повышается концентрация кетоновых тел (кетонемия и кетонурия).
Гиперинсулинизм – наблюдается при инсулиноме (опухоли, развивающейся из Р-клеток островков Лангерганса) и при передозировке инсулина в ходе лечения сахарного диабета. Основными симптомами являются гипогликемия (снижение концентрации глюкозы в крови), судороги, потеря сознания; при тяжелой гипогликемии может наступить смерть.
Глюкагон – гормон полипептидной природы, образуется в а- клетках островков Лангерганса поджелудочной железы. Особенно много глюкагона синтезируется при голодании, то есть глюкагон является главным гормоном, поддерживающим уровень глюкозы в крови при этом состоянии.
Главные ткани-мишени для глюкагона: печень, жировая ткань, корковое вещество почек, сердечная (но не скелетная) мышца.
В печени гормон стимулирует распад гликогена до глюкозы в течение первых суток голодания. Но, так как запасы гликогена в печени полностью исчезают через сутки, то, начиная со вторых суток голодания, глюкагон активирует в печени глюконеогенез, то есть синтез глюкозы из аминокислот, образующихся при распаде белка. Таким образом, благодаря двум указанным механизмам (увеличению распада гликогена и активации глюконеогенеза в печени), глюкагон поддерживает концентрацию глюкозы в крови во время голодания.
В отличие от адреналина, глюкагон не действует на гликоген мышц.?
Также в печени глюкагон ингибирует гликолиз, снижает синтез гликогена и жирных кислот, но активирует синтез кетоновых тел.
В жировой ткани глюкагон увеличивает распад жира и тормозит его синтез.
В корковом веществе почек глюкагон активирует глюконеогенез.
Во всех тканях-мишенях глюкагон увеличивает распад белка, уменьшает его синтез.
Патология. Глюкагонома – опухоль островков Лангерганса, состоящая преимущественно из а-клеток.
Гормоны мозгового вещества надпочечников
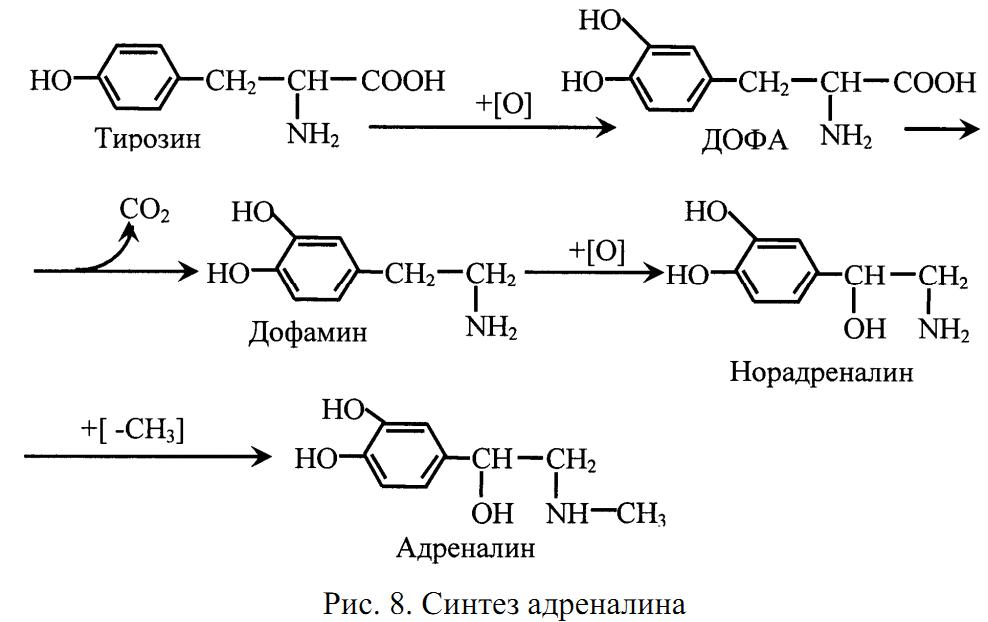
В мозговом веществе надпочечников вырабатываются адреналин и норадреналин. Они образуются из аминокислоты тирозина (рис. 8).
Биохимические особенности адреналина и норадреналина
1. Наибольшая секреция адреналина наблюдается при стрессе и физической нагрузке
2. На адреналин и норадреналин организм реагирует очень быстро.
3. Адреналин и норадреналин готовят организм к выполнению быстрой и интенсивной работы.
4. Адреналин может действовать через в- и через а-рецепторы. Норадреналин действует в основном на а-рецепторы.
5. Мозговое вещество надпочечников секретирует в кровь как адреналин, так и норадреналин. Вне мозгового вещества надпочечников адреналин нигде не образуется. Норадреналин образуется еще в окончаниях симпатических нервов (является медиатором симпатической нервной системы).
В норме только очень небольшая часть адреналина выделяется с мочой (1–5 %). Это количество столь мало, что не обнаруживается обычными лабораторными методами, поэтому считается, что в норме адреналин в моче отсутствует.
Распад адреналина и норадреналина происходит в печени (рис. 9. . При этом образуются метоксинорадреналин глюкуронид и метоксиадреналин глюкуронид, составляющие 30 % от всех продуктов распада адреналина и норадреналина, а остальное количество приходится на ванилилминдальную кислоту (ВМК), которая используется для диагностики.
Главные ткани-мишени для адреналина – печень, мышцы, жировая ткань и сердечно-сосудистая система.
В печени гормон увеличивает распад гликогена до глюкозы и повышает её концентрацию в крови.
В мышцах адреналин является стимулятором распада гликогена до глюкозо-6-фосфата, который не может выйти из клетки в кровь, а утилизируется по пути гликолиза с образованием молочной кислоты. Таким образом, в отличие от печени, при распаде гликогена в мышцах никогда не образуется свободная глюкоза.
В жировой ткани гормон увеличивает распад жира до жирных кислот, что сопровождается повышением их концентрации в крови.
Действие адреналина на сердечно-сосудистую систему проявляется в том, что он увеличивает силу и частоту сердечных сокращений, повышает артериальное давление, сужает артериолы кожи, слизистых оболочек и приносящие артериолы клубочков почек (поэтому при стрессе наблюдаются бледность и анурия – прекращение образования мочи), но расширяет сосуды сердца, мышц и внутренних органов. Действуя через систему кровообращения, адреналин затрагивает практически все функции всех органов, в результате чего мобилизуются силы организма для противодействия стрессовым ситуациям.
Кроме указанных эффектов, адреналин расслабляет гладкую мускулатуру бронхов, кишечника, тела мочевого пузыря, но сокращает сфинктеры желудочно-кишечного тракта, мочевого пузыря, мышцы, поднимающие волосы на коже, расширяет зрачок.
Патология
Состояния, связанные с гипофункцией мозгового вещества надпочечников, не описаны. Гиперфункция этой структуры возникает при опухоли феохромоцитоме. Содержание адреналина в крови увеличивается в 500 и более раз. Наблюдается повышение артериального давления, в крови резко увеличивается концентрация жирных кислот и глюкозы. В моче появляется адреналин и глюкоза (в норме в моче они не определяются обычными методами), значительно увеличивается содержание ВМК.
Гормоны коры надпочечников
В коре надпочечников образуются из холестерина стероидные гормоны:кортикостероиды (глюкокортикоиды и минералокортикоиды) и половые гомоны (женские и мужские).
Биохимические особенности коры надпочечников
В расчете на 1 грамм ткани кора надпочечников занимает второе место в организме после головного мозга по содержанию холестерина и первое место – по содержанию аскорбиновой кислоты (витамина С), необходимой для превращения холестерина в стероидные гормоны.
Распад стероидных гормонов
Обезвреживание стероидных гормонов происходит в печени двумя путями.
1. Около 90 % стероидных гормонов сначала восстанавливается, затем конъюгирует с глюкуроновой кислотой и легко экскретируется с мочой.
2. У 10 % глюкокортикоидов, минералокортикоидов и мужских (но не женских) половых гормонов происходит отщепление боковой цепи у 17-го углеродного атома и его окисление с образованием кетогруппы, в результате чего образуются 17-кетостероиды (17-КС), которые также выделяются с мочой в связанном с глюкуроновой кислотой виде. Таким образом, 17-КС – это не гормоны, а продукты распада гормонов: глюкокортикоидов, минералокортикоидов и мужских (но не женских) половых гормонов.
Глюкокортикоиды
Представителями глюкокортикоидов являются гидрокортизон (кортизол, рис. 10. , кортизон и кортикостерон.
Ткани-мишени для этой группы гормонов: печень, мышцы, жировая, лимфоидная и соединительная ткани. Причем в печени глюкокортикоиды повышают проницаемость мембран для транспорта веществ в клетку и активируют анаболические процессы (то есть синтез веществ), а в остальных тканях – понижают проницаемость мембран и стимулируют катаболизм (то есть распад веществ).
Действие глюкокортикоидов на метаболизм
Углеводный обмен. Во всех тканях-мишенях глюкокортикоиды тормозят гликолиз. В печени гормоны усиливают глюконеогенез и синтез гликогена, в остальных тканях – уменьшают транспорт глюкозы в клетку, в мышцах – снижают синтез гликогена.
При избытке глюкокортикоидов (применение их для лечения в больших дозах или длительно, а также повышенное образование глюкокортикоидов в организме) развивается гипергликемия вследствие активации глюконеогенеза в печени и понижения утилизации глюкозы в периферических тканях. Длительная гипергликемия может привести к срыву инсулярного аппарата поджелудочной железы и развитию стероидного диабета.?
Липидный обмен. В печени глюкокортикоиды повышают синтез триглицеридов, липопротеинов очень низкой плотности (ЛПОНП) и кетоновых тел. В жировой ткани гормоны увеличивают распад жира на конечностях, но усиливают отложение жира на туловище и лице. Поэтому при избытке глюкокортикоидов наблюдается так называемое паукообразное ожирение и повышение уровня кетоновых тел в крови.
Белковый обмен. В печени глюкокортикоиды увеличивают синтез белка, в остальных тканях – снижают синтез и стимулируют распад тканевых белков. В связи с этим при избытке глюкокортикоидов наблюдаются замедление заживления ран, атрофия и слабость мышц, в костях – остеопороз (разрежение кости, что сопровождается легко возникающими переломами, например, компрессионными переломами позвонков и длинных костей уже при минимальной травме).
В лимфоидной ткани избыток глюкокортикоидов приводит к угнетению синтеза антител и уменьшению образования лимфоцитов, поэтому при стрессе (когда вырабатывается много глюкокортикоидов) снижается иммунная защита организма и повышается восприимчивость к инфекционным заболеваниям. Указанный механизм действия глюкокортикоидов на лимфоидную ткань лежит в основе их применения при лечении аллергии и при трансплантации для подавления реакции отторжения пересаженного органа.
Системное действие глюкокортикоидов
1. Глюкокортикоиды усиливают секрецию HCl в желудке. Механизм их действия обусловлен тем, что глюкокортикоиды тормозят синтез простагландинов, которые снижают секрецию HCl, поэтому при избытке глюкокортикоидов в организме могут развиваться стероидные язвы желудка.
2. Глюкокортикоиды обладают противовоспалительным действием. Они воздействуют на все стадии воспалительного процесса, но особенно сильно снижают проницаемость мембран и ингибируют синтез простагландинов, которые являются тканевыми факторами воспаления, поэтому применение глюкокортикоидов возможно для лечения воспалений.
3. Глюкокортикоиды снижают повышенную реактивность организма, т.е. гиперчувствительность, поэтому используются при лечении аллергии, и, в частности, анафилактического шока.
4. Глюкокортикоиды повышают устойчивость организма к повреждающим факторам (травмы, инфекции, интоксикации, боль, холод, физическая нагрузка, тяжелые психические потрясения).
5. Глюкокортикоиды оказывают пермиссивное действие на организм, т.е. усиливают действие других гормонов.
Минералокортикоиды
Представителями минералокортикоидов являются альдостерон (рис. 11) и дезоксикортикостерон. Они регулируют обмен натрия,
Главной тканью-мишенью для действия гормонов является эпителий дистальных канальцев почек, где альдостерон увеличивает реабсорбцию натрия из мочи в кровь. Поэтому альдостерон называют натрийзадерживающим гормоном. Поскольку натрий «тянет» за собой воду, то при избытке минералокортикоидов в организме повышается артериальное давление, усиливаются отеки и воспалительные процессы.
Одновременно с увеличением реабсорбции натрия под действием альдостерона возрастает экскреция калия с мочой. Поэтому при избытке гормона в организме снижается концентрация калия в крови, что приводит к повышению возбудимости миокарда, нарушению работы сердца, возникают сильная слабость, характерные изменения на ЭКГ, и может развиться сердечная недостаточность.
Другой тканью-мишенью для минералокортикоидов являются потовые железы. В жару альдостерон препятствует чрезмерной потере натрия с потом.
При недостаточном синтезе альдостерона натрий теряется с мочой, что приводит к потере воды, т.е. дегидратации организма.
Глюкокортикоиды обладают частичным действием минералокортикоидов, поэтому при длительном применении с лечебной целью глюкокортикоидов больным обязательно назначают препараты калия.
Нарушения гормональной функции коры надпочечников
Гиперфункция коры надпочечников, или гиперкортицизм, может проявляться либо повышенной секрецией всех групп гормонов, либо преимущественно одной из групп гормонов. В последнем случае выделяют 3 вида гиперкортицизма.
1. Синдром Иценко-Кушинга (опухоль пучковой зоны коры надпочечников, синтезирующая, главным образом, кортизол) и болезнь Иценко-Кушинга (неопухолевая гиперплазия, то есть разрастание, коры надпочечников под влиянием избыточной секреции кортикотропина гипофизом).
2. Первичный альдостеронизм, или болезнь Конна – избыточное образование минералокортикоидов в организме (в клубочковой зоне коры надпочечников).
3. Адреналовый вирилизм, или адреногенитальный синдром – сопровождается гиперсекрецией мужских половых гормонов в сетчатой зоне коры надпочечников. При этом у женщин наблюдается появление мужских признаков, у мужчин – усиление мужских признаков, у детей – преждевременное половое созревание.
Гипокортицизм, называемый Аддисоновой, или бронзовой болезнью, сопровождается дефицитом глюко- и минералокортикоидов и смешанными изменениями обмена веществ и функций организма. Причиной гипокортицизма может явиться туберкулёз или атрофия коры надпочечников. Недостаточное образование кортикостероидов приводит к сильной слабости, утомляемости, снижению артериального давления, наблюдаются пигментации кожи, тяга к соленой пище, высокая чувствительность к стрессам и инфекциям, непереносимость голода из-за выраженной гипогликемии. В крови снижается концентрация натрия и увеличивается концентрация калия.
Гормоны половых желёз
Женские половые гормоны
Женские половые гормоны представлены эстрогенами и прогестинами (гестагенами).
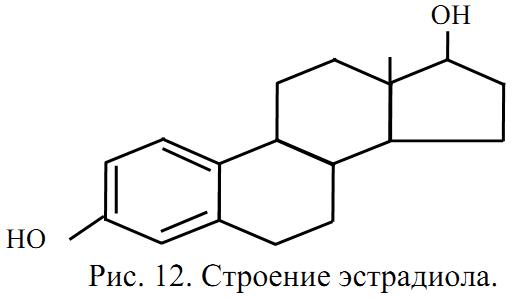
К эстрогенам относятся: эстрадиол (рис. 12) образуется в фолликулах яичников), эстриол (гормон плаценты) и эстрон (синтезируется в коре надпочечников). Представителем прогестинов является прогестерон, который вырабатывается в желтом теле яичников. Небольшое количество женских половых гормонов вырабатывается в организме мужчин.
Ткани, чувствительные к действию эстрогенов, делятся на 2 группы: половые органы и неполовые органы.
Действие женских половых гормонов на половые органы
В половых органах женские половые гормоны способствуют развитию и функционированию этих органов и формированию вторичных половых признаков в период полового созревания.
В матке увеличивается рост железистого эпителия эндометрия и гладкой мускулатуры миометрия, усиливается васкуляризация органа.
Во влагалище увеличивается число слоев клеток, что является диагностическим критерием действия эстрогенов на организм.
В молочной железе эстрогены стимулируют рост протоков, прогестерон – рост железистой ткани.
Действие женских половых гормонов на неполовые органы
В неполовых органах эстрогены оказывают также характерное действие.
ЦНС, гипоталамус, гипофиз – под влиянием гормонов происходит формирование типичного полового поведения, инстинкта, психики женщины.
Кости, хрящи, гортань – эстрогены способствуют формированию характерного «женского» типа скелета, гортани и голоса. Эстрогены ускоряют окостенение эпифизов, где находятся зоны роста кости, поэтому, если у девочки в период полового созревания образуется мало эстрогенов, замедляется окостенение эпифизов, и в этом случае девочка может иметь необычно высокий рост. У взрослых женщин при продолжительном введении эстрогенов или их избыточном образовании в организме происходит интенсивное обызвествление костей, и могут исчезать полости, в которых находится костный мозг, что приводит к развитию анемии.
Кожа – эстрогены способствуют росту волос по женскому типу, тормозят рост волос на коже, снижают секреторную активность сальных желез (понижают сальность кожи).
Печень – эстрогены стимулируют синтез специфических белков печени: ангиотензиногена, способствующего повышению артериального давления, и некоторых факторов свертывания крови (II, VII, IX, X). Поэтому при избытке эстрогенов в организме наблюдается склонность к гипертонии и тромбозам.
Кроме этого, эстрогены, воздействуя на печень, увеличивают образование в ней липопротеинов очень низкой плотности (ЛПОНП) и липопротеинов высокой плотности (ЛПВП). ЛПОНП на 50 % состоят из триглицеридов (нейтрального жира), из печени они через кровь доставляются в жировую ткань, где жир откладывается. Поэтому у женщин мышцы всегда покрыты слоем подкожного жира. ЛПВП уменьшают концентрацию холестерина в крови, способствуют его выведению из организма. Поэтому женщины реже, чем мужчины, заболевают атеросклерозом и инфарктом миокарда.
Жировая ткань – в ней эстрогены и прогестерон увеличивают синтез жира, тормозят его расщепление, способствуют формированию типично женских жировых отложений.
Почки – эстрогены способствуют задержке натрия в организме, прогестерон усиливает потерю натрия с мочой. Поскольку при беременности образуется много прогестерона, натрий усиленно теряется организмом, отсюда – тяга к соленой пище.
Мужские половые гормоны
Мужские половые гормоны (андрогены) представлены тестостероном (рис. 13. и андростероном. Они образуются в семенниках, коре надпочечников, предстательной железе. Небольшое количество андрогенов синтезируется у женщин в яичниках.
Как и женские половые гормоны, андрогены действуют не только на половые, но и на неполовые органы.
Действие мужских половых гормонов на половые органы
В половых органах мужские половые гормоны оказывают андрогенное действие, то есть способствуют развитию и функционированию этих органов и формированию вторичных половых признаков в период полового созревания.
Действие мужских половых гормонов на неполовые органы
В неполовых органах андрогены обладают генерализованным анаболическим действием, то есть стимулируют синтез нуклеиновых кислот, белка, задерживают в организме азот и кальций, усиливают синтез фосфолипидов мембран.
ЦНС, гипоталамус, гипофиз – под влиянием андрогенов происходит формирование типичного полового поведения, инстинкта и психики мужчины, то есть образуются поведенческие особенности мужского пола. Андрогены влияют на развитие мозга. Если во внутриутробном периоде в критические стадии развития и дифференцировки мозга развивается недостаточность андрогенов, то в будущем у этого юноши или мужчины могут возникнуть варианты половой ориентации. Избыток андрогенов в организме способствует агрессивности.
Кости, хрящи, гортань – андрогены способствуют формированию характерных физиологических особенностей мужского скелета, гортани, голоса, усиливают отложение фосфорно-кальциевых солей в эпифизарных зонах роста. Чрезмерная выработка гормонов может приводить к преждевременному заращению эпифизов и развитию низкорослости.
Мышцы – андрогены увеличивают мышечную массу и силу, создают характерную рельефность мышц.
Кожа – андрогены обладают стимулирующим действием на сальные железы, повышая сальность кожи, усиливают пигментацию кожи (солнечный загар), увеличивают рост волос на лице и теле, способствуют росту волос по мужскому типу. Избыток гормонов может привести к облысению.
Жировая ткань – андрогены ускоряют расщепление жира в жировой ткани, тормозят его синтез.
В печени и почках андрогены резко увеличивают синтез белка, в кроветворных органах усиливают эритропоэз.
Анаболические стероиды
На основе мужских половых гормонов синтезированы аналоги этих соединений – анаболические стероиды, обладающие максимальной анаболической активностью и минимальной – андрогенной. Первоначально анаболические стероиды широко применяли для откорма скота. Однако анаболические стероиды очень плохо метаболизируют в организме животных и не разрушаются при термической обработке пищи. Поэтому, попадая с мясом в организм человека, анаболические стероиды вызывали тяжелые поражения печени, в том числе опухоли, поскольку продукты превращения этих соединений являются канцерогенами.
В настоящее время применение анаболических стероидов в практике животноводства уменьшилось. Однако некоторые спортсмены продолжают применять этих средства для повышения спортивных результатов. Тем не менее, установлено, что даже относительно кратковременное (в течение 2 лет) применение анаболиков в возрастном периоде с 18 до 26 лет (кроме перечисленных опасностей для здоровья спортсмена) может привести у мужчин к ранней импотенции, а у женщин – к раку молочной железы.
Небольшие дозы анаболических стероидов применяют в лечебной практике у лиц после 35 лет при тяжелых травмах, инфаркте миокарда, после операций для ускорения заживления ран, увеличения массы тела и улучшения аппетита при истощении.
Центральная регуляция эндокринной системы
Гормоны оказывают многообразное биологическое действие на организм. Синтез самих гормонов и выделение их в кровь, в свою очередь, регулируются потребностями организма. О потребностях организма сообщают импульсы, идущие от рецепторов по афферентным нервным волокнам в ЦНС. Там информация перерабатывается, и по эфферентным нервным волокнам импульсы идут на периферию. Однако нервная регуляция не охватывает функции всех клеток организма, поэтому дополняется гормональной регуляцией. Местом, где соединяются нервная и гормональная регуляции, является гипоталамус.
Нервные импульсы, идущие из ЦНС, приводят к образованию в гипоталамусе коротких пептидов, которые называются либеринами и статинами. Эти пептиды синтезируются в очень небольшом количестве и по системе портального кровообращения гипофиза переносятся к его клеткам (аденогипофизу). Здесь под влиянием либеринов активируется, а под влиянием статинов тормозится синтез тропных гормонов гипофиза. Выделяясь в кровоток, тропные гормоны достигают периферических эндокринных желёз, и там способствуют синтезу и выделению в кровь гормонов, которые и оказывают своё биологическое действие.
Гормоны гипофиза
В передней и средней доле гипофиза (аденогипофиз) образуются тропные гормоны. Задняя доля гипофиза (нейрогипофиз) только секретирует гормоны (вазопрессин и окситоцин), которые синтезируются в ядрах гипоталамуса.
Передняя доля гипофиза
АКТГ – адренокортикотропный гормон, или кортикотропин. Действует, главным образом, на пучковую зону коры надпочечников, где образуются, в основном, глюкокортикоиды. Кроме того, АКТГ усиливает расщепление гликогена в печени и жиров – в жировой ткани.
ТТГ – тиреотропный гормон, или тиреотропин. Регулирует развитие и функционирование щитовидной железы, синтез и секрецию в кровь тиреоидных гормонов.
ГТГ – гонадотропные гормоны, или гонадотропины. К ним относятся фолликулостимулирующий гормон (ФСГ, или фоллитропин) и лютеинизирующий гормон (ЛГ, или лютропин). ФСГ вызывает созревание фолликулов в яичниках у женщин и сперматогенез у мужчин. ЛГ стимулирует у женщин секрецию эстрогенов и прогестерона, вызывает образование желтого тела в яичниках, а у мужчин – секрецию тестостерона.
ЛТГ – лактотропный гормон, или пролактин. Стимулирует развитие молочных желез и лактацию у женщин, способствует формированию родительских инстинктов; у мужчин снижает половую потенцию.
Липотропные гормоны (липотропины) – оказывают жиромобилизующее действие (увеличивают распад жира).
СТГ – соматотропный гормон, или соматотропин, иначе называется «гормон роста». Особенностью гормона является его сильно выраженная видовая специфичность. Это значит, что СТГ животных не действует на человека.
Стимуляторами секреции гормона являются:
1. сон, особенно в первые часы после засыпания (если ребёнок мало спит, он плохо растет);
2. холод (в целом, северяне выше южан);
3. стресс (если ребенка ограждать от нормальных повседневных стрессов, он будет отставать в росте);
4. физическая нагрузка (в целом, спортсмены выше лиц, избегающих регулярных физических нагрузок).
Ткани-мишени для СТГ – все клетки организма.
1. Анаболическое. В клетках СТГ увеличивает синтез ДНК, РНК и белка, стимулирует рост костей (остеогенез), хрящей (хондрогенез) и мягких тканей, регулирует процессы роста и развития скелета и всего организма, приводит к увеличению размеров тела. Хрящевая ткань эпифизов наиболее чувствительна к действию СТГ, за счет этого происходит рост трубчатых костей в длину.
2. Диабетогенное. В печени СТГ активирует глюконеогенез (через стимуляцию секреции глюкагона). В мышцах и жировой ткани СТГ уменьшает проницаемость мембран для транспорта аминокислот в клетку. При избытке СТГ повышается концентрация глюкозы в крови и развивается инсулинорезистентность периферических тканей, т.е. соматотропный диабет.
3. Липолитическое. У детей в период интенсивного роста отсутствуют жировые отложения, так как в жировой ткани СТГ усиливает распад жира до жирных кислот. Жирные кислоты поступают в кровь и утилизируются в тканях. При избытке СТГ в крови значительно увеличивается концентрация жирных кислот, и они усиленно используются печенью по 2 направлениям:
• на синтез жира (поэтому при избытке СТГ развивается жировое перерождение печени);
• на бета-окисление, в результате чего образуется ацетил-КоА, который используется на образование кетоновых тел; поэтому при избытке СТГ повышается концентрация кетоновых тел в крови.
Патология
При недостатке выработки СТГ (гипофизарная карликовость, или нанизм) отмечается пропорциональное недоразвитие всего тела, низкий рост, но, в отличие от кретинизма, нет признаков деформации скелета и умственной отсталости.
Гиперсекреция СТГ возникает при опухолях аденогипофиза. Если такое состояние развивается в детском возрасте, до завершения окостенения скелета, наблюдается гигантизм, признаками которого являются чрезмерный рост скелета и непропорционально длинные конечности. Если гиперсекреция СТГ возникает у взрослых, то есть после завершения роста скелета, наблюдается акромегалия. Это заболевание характеризуется непропорционально интенсивным ростом отдельных частей скелета (кистей, стоп, подбородка, надбровных дуг, носа), разрастанием мягких тканей лица (губ, носа, языка), а также увеличением желез внутренней секреции, что может сопровождаться их гиперфункцией.
Средняя доля гипофиза
МСГ – меланоцитостимулирующие гормоны, или меланотропины. Увеличивают количество пигментных клеток (меланоцитов) и стимулируют выработку пигмента меланина в коже, радужке и сетчатке глаза.
Задняя доля гипофиза
Окситоцин и вазопрессин лишь условно относят к гормонам задней доли гипофиза, поскольку они синтезируются в особых нейронах гипоталамуса (в супраоптическом и паравентрикулярном ядрах). По отросткам нейронов эти гормоны поступают в заднюю долю гипофиза, где депонируются и откуда непосредственно выделяются в кровь.
Окситоцин является стимулятором гладкой мускулатуры матки при родах.
Вазопрессин, или антидиуретический гормон, вызывает сокращение гладкой мускулатуры сосудов, что приводит к сужению сосудов и повышению артериального давления. Помимо этого, вазопрессин оказывает мощное антидиуретическое действие – стимулирует обратное всасывание (реабсорбцию) воды в почках и уменьшает объем выделяемой мочи. При атрофии задней доли гипофиза развивается несахарный диабет – заболевание, при котором наблюдается выделение чрезвычайно больших количеств жидкости с мочой (10 – 20 л в сутки).
Использование гормонов в медицине
Гормоны в медицине применяются, в основном, по следующим направлениям.
1. Заместительная терапия: гормоны как лекарственные препараты используются при гипофункции эндокринных желез.
2. Использование механизмов действия гормонов на биохимические процессы и функции.
Например, окситоцин используют для стимуляции родовой деятельности, адреналин – для повышения артериального давления, глюкокортикоиды – для лечения воспалений и как противоаллергическое средство, половые гормоны – для лечения некоторых гормональнозависимых опухолей (эстрогены – для лечения рака предстательной железы, андрогены – для лечения рака молочной железы).
3.Использование аналогов гормонов: на основе женских половых гормонов созданы пероральные контрацептивы (противозачаточные средства), на основе мужских половых гормонов созданы анаболические стероиды.
Простагландины и другие эйкозаноиды
Название эйкозаноиды происходит от эйкозатетраеновой (арахидоновой) кислоты, из которой эти соединения образуются. Эйкозаноиды называют гормоноподобными веществами, а также местными или тканевыми гормонами, потому что, в отличие от истинных гормонов, которые образуются в одних органах (эндокринных железах), а действуют в других (тканях-мишенях), эйкозаноиды действуют там же, где и синтезируются.
Синтез эйкозаноидов
Эйкозаноиды образуются из арахидоновой кислоты, которая отщепляется от фосфолипидов мембран под действием фосфолипазы А2. Арахидоновая кислота может превращаться по 2 путям (рис. 14. : циклооксигеназному, главным ферментом которого является циклооксигеназа (простагландинсинтетаза), и липоксигеназному, с участием липоксигеназы. В результате циклооксигеназного пути превращения арахидоновой кислоты образуются простагландины, простациклины и тромбоксаны. В липоксигеназном пути синтезируются лейкотриены. Ингибиторы указанных ферментов применяются для уменьшения синтеза эйкозаноидов в тканях.
Лейкотриены – участвуют в воспалении, аллергии, иммунитете, привлекают лейкоциты в очаг воспаления, сужают бронхи, увеличивают секрецию бронхиальной слизи.
Простациклины – расширяют сосуды, снижают артериальное давление, препятствуют агрегации (слипанию) тромбоцитов, тем самым препятствуют тромбозам.
Тромбоксаны – способствуют слипанию тромбоцитов, тем самым способствуют тромбозам. Сильнее всех соединений сужают сосуды. Соотношение простациклин / тромбоксан в стенке сосудов имеет большое значение в развитии тромбозов.
Простагландины
Простагландины синтезируются во всех клетках, кроме эритроцитов. Разрушаются простагландины в организме очень быстро (через 20 мин), и продукты их распада выводятся с мочой.
Общим для действия простагландинов является то, что они, в основном, усиливают действие других гормонов через стимуляцию деятельности эндокринных желёз (гипофиз, щитовидная железа, поджелудочная железа, надпочечники).
Вместе с тем, различают 2 класса простагландинов: простагландины Е (PG E), растворимые в эфире, и простагландины F (PG F), растворимые в фосфатном буфере. Каждый из классов делится на подклассы, обозначаемые индексом, например, PG E1, PG E2, и т.д., и буквами греческого алфавита, например, PG F2a.
Действие простагландинов Е
1. Тормозят распад жира и гликогена.
2. Являются тканевыми факторами воспаления: вырабатываются в большом количестве в очаге воспаления, увеличивают проницаемость сосудов и клеточных мембран при воспалении, расширяют капилляры. PG E являются сильными пирогенами (повышают температуру тела). Аспирин является ингибитором синтеза простагландинов, поэтому снижает температуру тела.
3. Вызывают пульсирующие головные боли, которые снимаются через 20 мин после приёма аспирина.
4. Расширяют сосуды, снижают артериальное давление, поэтому применяются при гипертонии.
5. Расширяют бронхи, поэтому применяются для лечения бронхиальной астмы.
6. Снижают секрецию HCl в желудке, препятствуют развитию язв, поэтому применяются при язве желудка. Аспирин и глюкокортикоиды уменьшают образование простагландинов, тормозящих секрецию HCl, поэтому длительное применение глюкокортикоидов или неправильный приём аспирина способствуют образованию язв.
7. В почках увеличивают выделение (объём) мочи и натрия.
Действие простагландинов F
1. Стимулируют перистальтику кишечника.
3. В матке стимулируют гладкую мускулатуру, поэтому применяются для прерывания беременности и как стимулятор родовой деятельности.
Источник статьи: http://www.sinref.ru/000_uchebniki/04600_raznie_2/158_Biohimiya-gormonov/000.htm
Биохимия гормонов (fb2)
Алла Анатольевна Масловская Биохимия гормонов
Список использованных сокращений
АКТГ – адренокортикотропный гормон
ВНД – высшая нервная деятельность
ВМК – ванилилминдальная кислота
ГТГ – гонадотропные гормоны
ЛГ – лютеинизирующий гормон
ЛПВП – липопротеины высокой плотности
ЛПОНП – липопротеины очень низкой плотности
МСГ – меланоцитостимулирующий гормон
СТГ – соматотропный гормон
Т4 – тетраиодтиронин (тироксин)
Фн – фосфат неорганический
ФСГ – фолликулостимулирующий гормон
цАМФ – циклический аденозинмонофосфат
цГМФ – циклический гуанозинмонофосфат
ЦНС – центральная нервная система
Введение
Имеющаяся в учебниках обширная информация по теме «Биохимия гормонов» не позволяет студентам, впервые изучающим этот раздел, правильно сориентироваться в выборе главных моментов для понимания биологических эффектов и молекулярных механизмов действия гормонов на организм. Целью настоящего издания является предоставление студентам информации о биохимии гормонов в более четкой и ясной форме, что будет способствовать овладению учебной дисциплиной.
Материал пособия содержит описание общих закономерностей действия гормонов на клетку, а также обоснование и объяснение молекулярных механизмов влияния гормонов на организм в норме и при патологических состояниях.
Предлагаемый учебный материал поможет студентам глубже понять значимость регуляторных механизмов для согласованной работы органов и систем, а также научиться разбираться в сущности биохимических процессов, лежащих в основе метаболических нарушений при патологии эндокринной системы.
Гормоны
Из всех биологически активных соединений и субстратов, принимающих участие в регуляции биохимических процессов и функций, особая роль принадлежит гормонам.
Слово «гормон» происходит из греческого языка и означает «возбуждать», «приводить в движение».
Гормоны – это органические вещества, которые образуются в тканях одного типа (эндокринные железы, или железы внутренней секреции), поступают в кровь, переносятся по кровяному руслу в ткани другого типа (ткани-мишени), где оказывают своё биологическое действие (т. е. регулируют обмен веществ, поведение и физиологические функции организма, а также рост, деление и дифференцировку клеток).
Классификация гормонов
По химической природе гормоны делятся на следующие группы:
1. пептидные – гормоны гипоталамуса, гипофиза, инсулин, глюкагон, гормоны паращитовидных желез;
2. производные аминокислот – адреналин, тироксин;
3. стероидные – глюкокортикоиды, минералокортикоиды, мужские и женские половые гормоны;
4. эйкозаноиды – гормоноподобные вещества, которые оказывают местное действие; они являются производными арахидоновой кислоты (полиненасыщенная жирная кислота).
По месту образования гормоны делятся на гормоны гипоталамуса, гипофиза, щитовидной железы, паращитовидных желёз, надпочечников (коркового и мозгового вещества), женские половые гормоны, мужские половые гормоны, местные или тканевые гормоны.
По действию на биохимические процессы и функции гормоны делятся на:
1. гормоны, регулирующие обмен веществ (инсулин, глюкагон, адреналин, кортизол);
2. гормоны, регулирующие обмен кальция и фосфора (паратиреоидный гормон, кальцитонин, кальцитриол);
3. гормоны, регулирующие водно-солевой обмен (альдостерон, вазопрессин);
4. гормоны, регулирующие репродуктивную функцию (женские и мужские половые гормоны);
5. гормоны, регулирующие функции эндокринных желёз (адренокортикотропный гормон, тиреотропный гормон, лютеинизирующий гормон, фолликулостимулирующий гормон, соматотропный гормон);
6. гормоны стресса (адреналин, глюкокортикоиды и др.);
7. гормоны, влияющие на ВНД (память, внимание, мышление, поведение, настроение): глюкокортикоиды, паратиреоидный гормон, тироксин, адренокортикотропный гормон)
Свойства гормонов
Высокая биологическая активность. Концентрация гормонов в крови очень мала, но их действие сильно выражено, поэтому даже небольшое увеличение или уменьшение уровня гормона в крови вызывает различные, часто значительные, отклонения в обмене веществ и функционировании органов и может привести к патологии.
Короткое время жизни, обычно от нескольких минут до получаса, после чего гормон инактивируется или разрушается. Но с разрушением гормона его действие не прекращается, а может продолжаться в течение часов и даже суток.
Дистантность действия. Гормоны вырабатываются в одних органах (эндокринных железах), а действуют в других (тканях- мишенях).
Высокая специфичность действия. Гормон оказывает своё действие только после связывания с рецептором. Рецептор – это сложный белок-гликопротеин, состоящий из белковой и углеводной частей. Гормон связывается именно с углеводной частью рецептора. Причём строение углеводной части имеет уникальную химическую структуру и соответствует пространственному строению гормона. Поэтому гормон безошибочно, точно, специфично связывается только со своим рецептором, несмотря на малую концентрацию гормона в крови.
Не все ткани одинаково реагируют на действие гормона. Высокой чувствительностью к гормону обладают те ткани, в которых имеются рецепторы к данному гормону. В таких тканях гормон вызывает наиболее выраженные сдвиги в обмене веществ и функциях. Если рецепторы к гормону есть во многих, или почти во всех тканях, то такой гормон оказывает общее действие (тироксин, глюкокортикоиды, соматотропный гормон, инсулин). Если рецепторы к гормону присутствуют в весьма ограниченном числе тканей, то такой гормон обладает избирательным действием. Ткани, в которых имеются рецепторы к данному гормону, называются ткани-мишени. В тканях-мишенях гормоны могут воздействовать на генетический аппарат, мембраны, ферменты.
Типы биологического действия гормонов
1. Метаболическое – действие гормона на организм проявляется регуляцией обмена веществ (например, инсулин, глюкокортикоиды, глюкагон).
2. Морфогенетическое – гормон действует на рост, деление и дифференцировку клеток в онтогенезе (например, соматотропный гормон, половые гормоны, тироксин).
3. Кинетическое или пусковое – гормоны способны запускать функции (например, пролактин – лактацию, половые гормоны – функцию половых желёз).
4. Корригирующее. Гормонам принадлежит важнейшая роль в адаптации человека к различным факторам внешней среды. Гормоны изменяют обмен веществ, поведение и функции органов так, чтобы приспособить организм к изменившимся условиям существования, т.е. осуществляют метаболическую, поведенческую и функциональную адаптацию, тем самым поддерживают постоянство внутренней среды организма.
Механизм действия пептидных гормонов и адреналина
Рецепторы к этим гормонам находятся на наружной поверхности клеточной мембраны, и гормон внутрь клетки не проникает. Действие гормона в клетку передается при помощи так называемых вторых посредников, к которым относятся циклический АМФ (цАМФ), циклический ГМФ (цГМФ), кальций, инозитолтрифосфат, диацилглицерол (диглицерид) и некоторые другие. В системе передачи регуляторного сигнала они называются вторыми посредниками, потому что первым посредником является сам гормон.
Каждый из вторых посредников активирует специфическую протеинкиназу. Протеинкиназы фосфорилируют ферменты, и это изменяет активность ферментов.
Главным вторым посредником является цАМФ (рис. 1). Большинство гормонов действует через него. Другие посредники, действуя через свои протеинкиназы, могут изменять содержание цАМФ в клетке путём повышения или снижения активности ферментов, синтезирующих или разрушающих цАМФ.
Циклический АМФ образуется в клетке из АТФ под действием аденилатциклазной системы (рис. 2). В состав аденилатциклазной системы входят: рецептор, G-белок и фермент аденилатциклаза. G- белок называется так потому, что он способен связывать гуаниловые нуклеотиды (ГТФ или ГДФ). Существует 2 разновидности G-белка: Gs – стимулирует аденилатциклазу и увеличивает образование цАМФ и Gi – ингибирует аденилатциклазу и уменьшает образование цАМФ.
Белки Gs и Gi оказывают своё активирующее или ингибирующее действие только когда находятся в! активном состоянии. G-белок активен, когда он связан с ГТФ, и наоборот, связанный с ГДФ, G- белок неактивен.
Пока гормон не действует на клетку, аденилатциклазная система неактивна; все её компоненты разобщены и с G-белком связан ГДФ. Однако после связывания гормона с рецептором происходит последовательное изменение конформации всех компонентов аденилатциклазной системы, G-белок обменивает ГДФ на ГТФ, переходит в активное состояние и активирует аденилатциклазу, которая из АТФ синтезирует цАМФ. Циклический АМФ, в свою очередь, активирует специфическую цАМФ-зависимую протеинкиназу (протеинкиназу А), которая фосфорилирует внутриклеточные ферменты, в результате чего изменяется активность ферментов.
Протеинкиназа состоит из 4 субъединиц (тетрамер), две из которых являются регуляторными, а две – каталитическими (рис. 3. . В таком виде протеинкиназа неактивна. При связывании протеинкиназой 4 молекул цАМФ происходит отсоединение (диссоциация) каталитических субъединиц, которые фосфорилируют белки (ферменты), изменяя их активность.
Разрушается цАМФ фосфодиэстеразой.
Циклический ГМФ образуется из ГТФ под действием гуанилатциклазы по аналогии с синтезом цАМФ. Циклический ГМФ активирует специфическую цГМФ-зависимую протеинкиназу или протеинкиназу G, которая фосфорилирует ферменты, что сопровождается изменением их активности. Разрушается цГМФ, как и цАМФ, фосфодиэстеразой.
Кальций
Концентрация Са2+ во внеклеточной жидкости в 10 000 раз больше, чем в цитоплазме. Такая концентрация кальция оказалась бы потенциально летальной для клетки. Клетка борется с избытком Са2+ в цитоплазме путём откачивания его наружу с помощью Са2+- АТФазы, расположенной в плазматической мембране.
Под действием гормонального сигнала концентрация Са2+ в клетке возрастает в 10 и более раз за счет притока Са2+ из внеклеточной жидкости, а также выхода Са2+ из ЭПР и митохондрий. В клетке Са2+ связывается с белком кальмодулином и активирует специфическую Са2+-кальмодулин-зависимую протеинкиназу. В ГЛ 2+ ответ на гормональный сигнал и повышение концентрации Са в клетке специфическая протеинкиназа катализирует фосфорилирование множества внутриклеточных ферментов, регулируя, тем самым, их активность.
Инозитолтрифосфат и диглицерид
Эти вторые посредники являются производными фосфолипида мембран, фосфатидилинозитола. Указанный фосфолипид фосфорилируется в мембране под действием фермента фосфатидилинозитолкиназы при участии 2 молекул АТФ (рис. 4. .
Образующийся фосфатидилинозитолдифосфат расщепляется под действием специфического мембраносвязянного фермента фосфолипазы С, в результате чего образуются два вторых посредника: диглицерид (диацилглицерол, ДАГ) и инозитолтрифосфат (ИФ3.)
Биологические эффекты этих двух вторых посредников реализуются по-разному. ДАГ активирует Са2+-зависимую протеинкиназу С, которая катализирует фосфорилирование внутриклеточных ферментов, изменяя их активность. ИФ3 связывается со специфическим рецептором на ЭПР, способствуя выходу из него Са2+ в цитоплазму. Далее Са2+ связывается с кальмодулином и активирует Са2+-кальмодулин-зависимую протеинкиназу, которая катализирует фосфорилирование ферментов, изменяя их активность (рис. 5.)

Механизм действия стероидных гормонов и тироксина
Рецепторы к этим гормонам находятся внутри клетки, в цитоплазме. Гормон легко и быстро проникает через мембрану внутрь клетки, взаимодействует с рецептором с образованием гормон-рецепторного комплекса. Этот комплекс переносится в ядро, где связывается с ядерным хроматином в определенном участке ДНК. С этого участка ДНК начинается синтез специфических мРНК, которые затем выходят в цитоплазму и служат матрицей для синтеза ферментов или других белков, необходимых клетке и обеспечивающих ответ клетки на действие гормона (рис. 6. .
Таким образом, под действием пептидных гормонов и адреналина в клетке изменяется активность ферментов; стероидные гормоны и тироксин приводят к изменению количества ферментов.
Гормоны щитовидной железы
В щитовидной железе синтезируются тиреоидные гормоны – тироксин (Т4. и трииодтиронин (Т3. . Для синтеза этих гормонов необходим иод, который активно захватывается из крови клетками фолликулов щитовидной железы. Тироксин и трииодтиронин являются производными аминокислоты тирозина. Тироксин содержит в своей молекуле 4 атома иода, в состав трииодтиронина входит 3 атома иода.
В клетках эпителия фолликулов щитовидной железы находится белок тиреоглобулин. Это гликопротеин, содержащий много остатков аминокислоты тирозина (около 3 % от массы белка). Синтез тиреоидных гормонов идет из тирозина и атомов иода именно в составе молекулы тиреоглобулина и включает 2 стадии. На апикальных мембранах клеток фолликулов сначала происходит иодирование тирозина с образованием моноиодтирозина (МИТ) и дииодтирозина (ДИТ). Следующим этапом является конденсация МИТ и ДИТ с образованием Т3 и Т4 (рис. 7. .
Такая иодированная молекула тиреоглобулина секретируется в просвет фолликула, в коллоид. Когда в щитовидную железу приходит сигнал в виде ТТГ (тиреотропного гормона), клетки фолликула захватывают капельки коллоида вместе с тиреоглобулином, ферменты лизосом протеазы гидролизуют белок до аминокислот, и готовые Т3 и Т4 поступают в кровь.
В крови тиреоидные гормоны связываются с белком- переносчиком и в таком виде транспортируются в ткани-мишени. Концентрация Т4 в крови в 10 раз больше, чем Т3, поэтому Т4 называют главной формой тиреоидных гормонов в крови. Но Т3 в 10 раз активнее, чем Т4.
Ткани-мишени для тиреоидных гормонов – это все ткани, кроме селезёнки и семенников.
В тканях-мишенях тиреоидные гормоны освобождаются от белка и поступают в клетку. В клетках 90 % Т4 теряет 1 атом иода и превращается в Т3. Таким образом, главной внутриклеточной формой гормона является Т3.
Действие тиреоидных гормонов на организм зависит от концентрации этих гормонов в крови: в физиологических дозах они оказывают анаболическое действие, в больших дозах – катаболическое.
Действие физиологических (нормальных) концентраций Т4
Главное действие физиологических концентраций тиреоидных гормонов направлено на синтез белка и на энергетический обмен.
Действие Т4 на синтез белка. Через рецепторы цитоплазмы гормон действует на хроматин ядра, в результате чего увеличивается синтез нуклеиновых кислот (ДНК, мРНК) и белка. Наработка новых молекул белка ускоряет рост, деление и дифференцировку клеток, что особенно важно для растущего организма.
Тиреоидные гормоны абсолютно необходимы для структурного, биохимического и функционального созревания мозга. Считают, что в ЦНС клетки продолжают делиться в течение 1–1,5 лет после рождения. Поэтому если в этот период или еще до рождения возникает дефицит тиреоидных гормонов (гипотиреоз), это приводит к снижению синтеза белка во всем организме и, в частности, в мозговой ткани, нарушается процесс дифференцировки коры больших полушарий и мозжечка, и развивается умственная и физическая отсталость. Гипотиреоз у детей называется кретинизм. Чем раньше возникает дефицит тиреоидных гормонов, тем сильнее это сказывается на задержке развития ЦНС. Поэтому, чрезвычайно важна ранняя диагностика гипотиреоза, чтобы своевременно назначить адекватное лечение и избежать умственной отсталости.
Действие Т4 на энергетический обмен. Тиреоидные гормоны активируют энергетический обмен, т.е. расходование и синтез АТФ. Поскольку одновременно активируются 2 противоположно направленных процесса, между ними сохраняется равновесие. Внешне это проявляется увеличением потребления кислорода тканями и образованием тепла для поддержания нормальной температуры тела.
Молекулярный механизм действия тиреоидных гормонов на энергетический обмен заключается в следующем. Тиреоидные гормоны увеличивают расходование АТФ на энергозависимые процессы, в результате чего образуется АДФ. АДФ является активатором цепи тканевого дыхания (ЦТД), где из АДФ вновь образуется АТФ, которая снова расходуется на энергозависимые процессы.
Из всех энергозависимых процессов наиболее энергоёмким процессом является работа по поддержанию электрохимического градиента концентрации ионов Na+ и K+ по обеим сторонам клеточной мембраны. В процессе жизнедеятельности любая клетка, и нервная клетка в частности, может находиться в состоянии покоя и функционирования. В покое концентрация K+ в клетке больше, чем Na+, снаружи – наоборот. При функционировании клетки K+ выходит из неё, Na+ – входит в клетку.
Чтобы вернуть клетку в состояние покоя, надо выкачать из неё Na+ и ввести K+. Работу по восстановлению исходной концентрации ионов в клетке выполняет фермент ^+,К+-АТФаза. Процесс идет с затратой энергии АТФ, в результате чего образуется АДФ и Фн. №+Д+-АТФаза содержится в мембране всех клеток и является важнейшим ферментом для нормального функционирования нервной ткани. Важно отметить, что на работу ^^^-АТФазы расходуется большая часть энергии клетки (от 20 до 80 %, в среднем 50 % клеточных запасов АТФ).
Тиреоидные гормоны стимулируют №+Д+-АТФазу, тем самым увеличивая расщепление АТФ и образование АДФ и Фн в цитоплазме. АДФ затем переносится из цитоплазмы в митохондрию, где АДФ активирует ЦТД и, таким образом, повышает синтез АТФ, который используется при функционировании ^^^-АТФазы.
Таким образом, тиреоидные гормоны одновременно увеличивают использование АТФ и его образование, т. е. поддерживают энергетическое равновесие в клетке.
Сохранение энергетического равновесия очень важно для поддержания электрохимического градиента Na+ и K+ по обеим сторонам клеточной мембраны. Это является основой для нормального функционирования нервной ткани, т.е. для координации процессов возбуждения и торможения в мозге. Благодаря участию тиреоидных гормонов, процессы возбуждения и торможения в мозге скоординированы. При избытке или дефиците тиреоидных гормонов нарушается энергетическое равновесие, нарушаются электрохимические процессы в ЦНС, что сопровождается определёнными мозговыми симптомами.
Действие высоких (избыточных) концентраций Т4
При гипертиреозе (тиреотоксикоз, или Базедова болезнь) в организме образуется избыточное количество тироксина. Большие концентрации гормона действуют на митохондрии, которые являются «энергетическими станциями» клетки. В митохондриях находится ЦТД, т.е. цепь переносчиков, которая окисляет субстраты при помощи кислорода и в которой образуется энергия. В норме часть этой энергии запасается в виде АТФ, а часть идет на образование тепла для поддержания нормальной температуры тела. Образование АТФ в ЦТД называется окислительным фосфорилированием. Большие концентрации тиреоидных гормонов разобщают ЦТД и окислительное фосфорилирование. В результате ЦТД работает, субстраты окисляются, энергия в ЦТД образуется, но из-за разобщения ЦТД и окислительного фосфорилирования энергия не запасается в виде АТФ, а рассеивается в виде тепла. Поэтому одним из характерных признаков гипертиреоза является повышение температуры тела. Поскольку образование АТФ при этом заболевании снижается, то наблюдается сильная слабость, так как АТФ необходим для мышечного сокращения и поддержания тонуса мускулатуры. Дефицит АТФ в организме приводит к усиленному распаду белков, углеводов и жиров тела (катаболическое действие больших концентраций тироксина), что сопровождается резким общим похуданием.
Кроме перечисленных симптомов, при гипертиреозе наблюдаются: увеличение щитовидной железы (зоб), пучеглазие (экзофтальм), увеличение частоты сердечных сокращений (тахикардия), возбужденность, беспокойство, нервозность, плаксивость, бессонница, эмоциональная лабильность, потливость, кожа становится влажной и горячей.
Гипофункция щитовидной железы (гипотиреоз) у взрослых называется микседема. Развиваются слизеподобный отек тканей, ожирение, выпадение волос и зубов, апатия, сонливость, психическая инертность, снижение интереса и инициативы, гиперхолестеринемия, жировое перерождение печени, речь становится медленной и невнятной, мимика невыразительной, кожа – сухая, бледная и холодная, снижается температура тела.
Гипофункция щитовидной железы (гипотиреоз) у детей называется кретинизм (см. выше).
Особой формой гипотиреоза является эндемический зоб. Он возникает при недостаточном содержании йода в воде и пище. Компенсаторно разрастается ткань щитовидной железы, но при отсутствии иода это не приводит к увеличению выработки тиреоидных гормонов.
Гормоны паращитовидных желёз
В паращитовидных железах образуется паратиреоидный гормон (паратгормон) и кальцитонин. Однако основное количество кальцитонина вырабатывается в щитовидной железе.
Паратгормон – это гормон белковой природы, который повышает содержание кальция (Са ) и снижает концентрацию фосфата (Р) в крови. Действие паратгормона направлено на следующие ткани-мишени:
1. кости – гормон увеличивает выход Са и Р из кости в кровь; тормозит синтез коллагена в остеобластах, увеличивает разрушение минеральной и органической части кости остеокластами и остеоцитами;
2. кишечник – увеличивает всасывание Са2+ и Р из кишечника в кровь;
3. почки – увеличивает реабсорбцию Са2+ из мочи в кровь, но увеличивает выведение Р с мочой.
Патология
Гиперпаратиреоз – повышенное образование паратгормона, возникающее при опухоли паращитовидных желёз. Так как Са2+ усиленно выходит из кости, то наблюдаются самопроизвольные переломы вследствие рассасывания костной ткани. Повышение концентрации Са2+ в крови приводит:
1. к окостенению внутренних органов, обызвествлению ушибов, кровоподтёков;
2. к понижению нервно-мышечной возбудимости, что проявляется как атрофия и слабость мышц, а также депрессией, нарушением памяти и внимания.
Избыток паратгормона резко увеличивает секрецию гастрина, что, в свою очередь, приводит к повышению секреции HCl и пепсина в желудке, поэтому при избытке паратгормона могут развиться язвы желудка.
Гипопаратиреоз – может наблюдаться после операций на щитовидной железе, когда по ошибке были удалены и паращитовидные железы, либо возникает у детей при инфекциях дыхательных путей. Такое состояние сопровождается снижением концентрации Са2+ в крови, что приводит к повышению нервно- мышечной возбудимости. У взрослых наблюдаются конвульсии, судороги, что характеризуется как тетания. У детей может возникнуть спазмофилия, т.е. состояние, когда ребенок во время плача внезапно синеет из-за спазма дыхательных мышц.
Кальцитонин – понижает концентрацию и Са2+, и Р в крови. Оказывает влияние на те же ткани-мишени, что и паратгормон, однако действие кальцитонина, в основном, противоположно эффектам паратгормона. Однако, как и паратгормон, кальцитонин увеличивает выведение Р с мочой.
Гормоны поджелудочной железы
Инсулин – гормон белковой природы, синтезируется в р-клетках островков Лангерганса, запасается в секреторных гранулах в связи с цинком и выделяется в кровь в ответ на повышение концентрации глюкозы в крови.
По чувствительности к инсулину все ткани можно разделить на 3 группы:
1. Главные ткани-мишени или абсолютно зависимые от инсулина ткани. Они обладают максимальной чувствительностью к инсулину. К этой группе относятся жировая ткань и мышцы. Глюкоза не проникает в эти ткани и не утилизируется в них в отсутствие инсулина.
2. Абсолютно независимые от инсулина ткани. К ним относятся головной мозг, эритроциты, слизистая оболочка (эпителий) тонкого кишечника, мозговое вещество почек, семенники. В клетки этих тканей глюкоза проникает легко даже в отсутствие инсулина и является для них единственным энергетическим субстратом. Эти ткани (клетки) выполняют важнейшие функции организма: мозг – центральную регуляцию, эритроциты – транспорт кислорода, почки – экскрецию, тонкий кишечник – питание, семенники – воспроизводство (размножение). Причем мозг потребляет 50 % всей глюкозы организма, почки и эритроциты – ещё 20 %. Таким образом, для организма оказывается чрезвычайно важным то, что основной метаболический фонд глюкозы и жизненно важные функции оказываются независимыми от инсулина.
3. Относительно зависимые от инсулина ткани. Это все остальные ткани. По чувствительности к инсулину они занимают промежуточное положение между тканями 1-ой и 2-ой группы.
Действие инсулина на внутриклеточный метаболизм
1. Инсулин – единственный гормон, снижающий концентрацию глюкозы в крови. Такой эффект гормона обусловлен следующими механизмами:
• инсулин увеличивает проницаемость мембран для транспорта глюкозы из крови в клетки;
• инсулин активирует использование глюкозы по пути гликолиза (окислительный распад глюкозы) и на синтез гликогена;
• инсулин тормозит распад гликогена (гликогенолиз) и глюконеогенез (процесс образования глюкозы из аминокислот).
2. Инсулин является универсальным анаболическим гормоном. Он усиливает процессы синтеза нуклеиновых кислот, белка, жиров, гликогена и тормозит их распад. Кроме того, анаболическое действие инсулина проявляется в том, что он активирует процессы, дающие энергию для синтезов (гликолиз, цикл трикарбоновых кислот).
Патология
Сахарный диабет – заболевание, обусловленное недостатком инсулина в организме. Наблюдается повышенное содержание глюкозы в крови (гипергликемия), может появляться глюкоза в моче (глюкозурия), усиливается распад (катаболизм) белков, жира, гликогена, тормозится их синтез, активируется глюконеогенез и резко снижается активность гликолиза. В крови и моче повышается концентрация кетоновых тел (кетонемия и кетонурия).
Гиперинсулинизм – наблюдается при инсулиноме (опухоли, развивающейся из Р-клеток островков Лангерганса) и при передозировке инсулина в ходе лечения сахарного диабета. Основными симптомами являются гипогликемия (снижение концентрации глюкозы в крови), судороги, потеря сознания; при тяжелой гипогликемии может наступить смерть.
Глюкагон – гормон полипептидной природы, образуется в а- клетках островков Лангерганса поджелудочной железы. Особенно много глюкагона синтезируется при голодании, то есть глюкагон является главным гормоном, поддерживающим уровень глюкозы в крови при этом состоянии.
Главные ткани-мишени для глюкагона: печень, жировая ткань, корковое вещество почек, сердечная (но не скелетная) мышца.
В печени гормон стимулирует распад гликогена до глюкозы в течение первых суток голодания. Но, так как запасы гликогена в печени полностью исчезают через сутки, то, начиная со вторых суток голодания, глюкагон активирует в печени глюконеогенез, то есть синтез глюкозы из аминокислот, образующихся при распаде белка. Таким образом, благодаря двум указанным механизмам (увеличению распада гликогена и активации глюконеогенеза в печени), глюкагон поддерживает концентрацию глюкозы в крови во время голодания.
В отличие от адреналина, глюкагон не действует на гликоген мышц.?
Также в печени глюкагон ингибирует гликолиз, снижает синтез гликогена и жирных кислот, но активирует синтез кетоновых тел.
В жировой ткани глюкагон увеличивает распад жира и тормозит его синтез.
В корковом веществе почек глюкагон активирует глюконеогенез.
Во всех тканях-мишенях глюкагон увеличивает распад белка, уменьшает его синтез.
Патология. Глюкагонома – опухоль островков Лангерганса, состоящая преимущественно из а-клеток.
Гормоны мозгового вещества надпочечников
В мозговом веществе надпочечников вырабатываются адреналин и норадреналин. Они образуются из аминокислоты тирозина (рис. 8).
Биохимические особенности адреналина и норадреналина
1. Наибольшая секреция адреналина наблюдается при стрессе и физической нагрузке
2. На адреналин и норадреналин организм реагирует очень быстро.
3. Адреналин и норадреналин готовят организм к выполнению быстрой и интенсивной работы.
4. Адреналин может действовать через в- и через а-рецепторы. Норадреналин действует в основном на а-рецепторы.
5. Мозговое вещество надпочечников секретирует в кровь как адреналин, так и норадреналин. Вне мозгового вещества надпочечников адреналин нигде не образуется. Норадреналин образуется еще в окончаниях симпатических нервов (является медиатором симпатической нервной системы).
В норме только очень небольшая часть адреналина выделяется с мочой (1–5 %). Это количество столь мало, что не обнаруживается обычными лабораторными методами, поэтому считается, что в норме адреналин в моче отсутствует.
Распад адреналина и норадреналина происходит в печени (рис. 9. . При этом образуются метоксинорадреналин глюкуронид и метоксиадреналин глюкуронид, составляющие 30 % от всех продуктов распада адреналина и норадреналина, а остальное количество приходится на ванилилминдальную кислоту (ВМК), которая используется для диагностики.
Главные ткани-мишени для адреналина – печень, мышцы, жировая ткань и сердечно-сосудистая система.
В печени гормон увеличивает распад гликогена до глюкозы и повышает её концентрацию в крови.
В мышцах адреналин является стимулятором распада гликогена до глюкозо-6-фосфата, который не может выйти из клетки в кровь, а утилизируется по пути гликолиза с образованием молочной кислоты. Таким образом, в отличие от печени, при распаде гликогена в мышцах никогда не образуется свободная глюкоза.
В жировой ткани гормон увеличивает распад жира до жирных кислот, что сопровождается повышением их концентрации в крови.
Действие адреналина на сердечно-сосудистую систему проявляется в том, что он увеличивает силу и частоту сердечных сокращений, повышает артериальное давление, сужает артериолы кожи, слизистых оболочек и приносящие артериолы клубочков почек (поэтому при стрессе наблюдаются бледность и анурия – прекращение образования мочи), но расширяет сосуды сердца, мышц и внутренних органов. Действуя через систему кровообращения, адреналин затрагивает практически все функции всех органов, в результате чего мобилизуются силы организма для противодействия стрессовым ситуациям.
Кроме указанных эффектов, адреналин расслабляет гладкую мускулатуру бронхов, кишечника, тела мочевого пузыря, но сокращает сфинктеры желудочно-кишечного тракта, мочевого пузыря, мышцы, поднимающие волосы на коже, расширяет зрачок.
Патология
Состояния, связанные с гипофункцией мозгового вещества надпочечников, не описаны. Гиперфункция этой структуры возникает при опухоли феохромоцитоме. Содержание адреналина в крови увеличивается в 500 и более раз. Наблюдается повышение артериального давления, в крови резко увеличивается концентрация жирных кислот и глюкозы. В моче появляется адреналин и глюкоза (в норме в моче они не определяются обычными методами), значительно увеличивается содержание ВМК.
Гормоны коры надпочечников
В коре надпочечников образуются из холестерина стероидные гормоны:кортикостероиды (глюкокортикоиды и минералокортикоиды) и половые гомоны (женские и мужские).
Биохимические особенности коры надпочечников
В расчете на 1 грамм ткани кора надпочечников занимает второе место в организме после головного мозга по содержанию холестерина и первое место – по содержанию аскорбиновой кислоты (витамина С), необходимой для превращения холестерина в стероидные гормоны.
Распад стероидных гормонов
Обезвреживание стероидных гормонов происходит в печени двумя путями.
1. Около 90 % стероидных гормонов сначала восстанавливается, затем конъюгирует с глюкуроновой кислотой и легко экскретируется с мочой.
2. У 10 % глюкокортикоидов, минералокортикоидов и мужских (но не женских) половых гормонов происходит отщепление боковой цепи у 17-го углеродного атома и его окисление с образованием кетогруппы, в результате чего образуются 17-кетостероиды (17-КС), которые также выделяются с мочой в связанном с глюкуроновой кислотой виде. Таким образом, 17-КС – это не гормоны, а продукты распада гормонов: глюкокортикоидов, минералокортикоидов и мужских (но не женских) половых гормонов.
Глюкокортикоиды
Представителями глюкокортикоидов являются гидрокортизон (кортизол, рис. 10. , кортизон и кортикостерон.
Ткани-мишени для этой группы гормонов: печень, мышцы, жировая, лимфоидная и соединительная ткани. Причем в печени глюкокортикоиды повышают проницаемость мембран для транспорта веществ в клетку и активируют анаболические процессы (то есть синтез веществ), а в остальных тканях – понижают проницаемость мембран и стимулируют катаболизм (то есть распад веществ).
Действие глюкокортикоидов на метаболизм
Углеводный обмен. Во всех тканях-мишенях глюкокортикоиды тормозят гликолиз. В печени гормоны усиливают глюконеогенез и синтез гликогена, в остальных тканях – уменьшают транспорт глюкозы в клетку, в мышцах – снижают синтез гликогена.
При избытке глюкокортикоидов (применение их для лечения в больших дозах или длительно, а также повышенное образование глюкокортикоидов в организме) развивается гипергликемия вследствие активации глюконеогенеза в печени и понижения утилизации глюкозы в периферических тканях. Длительная гипергликемия может привести к срыву инсулярного аппарата поджелудочной железы и развитию стероидного диабета.?
Липидный обмен. В печени глюкокортикоиды повышают синтез триглицеридов, липопротеинов очень низкой плотности (ЛПОНП) и кетоновых тел. В жировой ткани гормоны увеличивают распад жира на конечностях, но усиливают отложение жира на туловище и лице. Поэтому при избытке глюкокортикоидов наблюдается так называемое паукообразное ожирение и повышение уровня кетоновых тел в крови.
Белковый обмен. В печени глюкокортикоиды увеличивают синтез белка, в остальных тканях – снижают синтез и стимулируют распад тканевых белков. В связи с этим при избытке глюкокортикоидов наблюдаются замедление заживления ран, атрофия и слабость мышц, в костях – остеопороз (разрежение кости, что сопровождается легко возникающими переломами, например, компрессионными переломами позвонков и длинных костей уже при минимальной травме).
В лимфоидной ткани избыток глюкокортикоидов приводит к угнетению синтеза антител и уменьшению образования лимфоцитов, поэтому при стрессе (когда вырабатывается много глюкокортикоидов) снижается иммунная защита организма и повышается восприимчивость к инфекционным заболеваниям. Указанный механизм действия глюкокортикоидов на лимфоидную ткань лежит в основе их применения при лечении аллергии и при трансплантации для подавления реакции отторжения пересаженного органа.
Системное действие глюкокортикоидов
1. Глюкокортикоиды усиливают секрецию HCl в желудке. Механизм их действия обусловлен тем, что глюкокортикоиды тормозят синтез простагландинов, которые снижают секрецию HCl, поэтому при избытке глюкокортикоидов в организме могут развиваться стероидные язвы желудка.
2. Глюкокортикоиды обладают противовоспалительным действием. Они воздействуют на все стадии воспалительного процесса, но особенно сильно снижают проницаемость мембран и ингибируют синтез простагландинов, которые являются тканевыми факторами воспаления, поэтому применение глюкокортикоидов возможно для лечения воспалений.
3. Глюкокортикоиды снижают повышенную реактивность организма, т.е. гиперчувствительность, поэтому используются при лечении аллергии, и, в частности, анафилактического шока.
4. Глюкокортикоиды повышают устойчивость организма к повреждающим факторам (травмы, инфекции, интоксикации, боль, холод, физическая нагрузка, тяжелые психические потрясения).
5. Глюкокортикоиды оказывают пермиссивное действие на организм, т.е. усиливают действие других гормонов.
Минералокортикоиды
Представителями минералокортикоидов являются альдостерон (рис. 11) и дезоксикортикостерон. Они регулируют обмен натрия,
Главной тканью-мишенью для действия гормонов является эпителий дистальных канальцев почек, где альдостерон увеличивает реабсорбцию натрия из мочи в кровь. Поэтому альдостерон называют натрийзадерживающим гормоном. Поскольку натрий «тянет» за собой воду, то при избытке минералокортикоидов в организме повышается артериальное давление, усиливаются отеки и воспалительные процессы.
Одновременно с увеличением реабсорбции натрия под действием альдостерона возрастает экскреция калия с мочой. Поэтому при избытке гормона в организме снижается концентрация калия в крови, что приводит к повышению возбудимости миокарда, нарушению работы сердца, возникают сильная слабость, характерные изменения на ЭКГ, и может развиться сердечная недостаточность.
Другой тканью-мишенью для минералокортикоидов являются потовые железы. В жару альдостерон препятствует чрезмерной потере натрия с потом.
При недостаточном синтезе альдостерона натрий теряется с мочой, что приводит к потере воды, т.е. дегидратации организма.
Глюкокортикоиды обладают частичным действием минералокортикоидов, поэтому при длительном применении с лечебной целью глюкокортикоидов больным обязательно назначают препараты калия.
Нарушения гормональной функции коры надпочечников
Гиперфункция коры надпочечников, или гиперкортицизм, может проявляться либо повышенной секрецией всех групп гормонов, либо преимущественно одной из групп гормонов. В последнем случае выделяют 3 вида гиперкортицизма.
1. Синдром Иценко-Кушинга (опухоль пучковой зоны коры надпочечников, синтезирующая, главным образом, кортизол) и болезнь Иценко-Кушинга (неопухолевая гиперплазия, то есть разрастание, коры надпочечников под влиянием избыточной секреции кортикотропина гипофизом).
2. Первичный альдостеронизм, или болезнь Конна – избыточное образование минералокортикоидов в организме (в клубочковой зоне коры надпочечников).
3. Адреналовый вирилизм, или адреногенитальный синдром – сопровождается гиперсекрецией мужских половых гормонов в сетчатой зоне коры надпочечников. При этом у женщин наблюдается появление мужских признаков, у мужчин – усиление мужских признаков, у детей – преждевременное половое созревание.
Гипокортицизм, называемый Аддисоновой, или бронзовой болезнью, сопровождается дефицитом глюко- и минералокортикоидов и смешанными изменениями обмена веществ и функций организма. Причиной гипокортицизма может явиться туберкулёз или атрофия коры надпочечников. Недостаточное образование кортикостероидов приводит к сильной слабости, утомляемости, снижению артериального давления, наблюдаются пигментации кожи, тяга к соленой пище, высокая чувствительность к стрессам и инфекциям, непереносимость голода из-за выраженной гипогликемии. В крови снижается концентрация натрия и увеличивается концентрация калия.
Гормоны половых желёз
Женские половые гормоны
Женские половые гормоны представлены эстрогенами и прогестинами (гестагенами).
К эстрогенам относятся: эстрадиол (рис. 12) образуется в фолликулах яичников), эстриол (гормон плаценты) и эстрон (синтезируется в коре надпочечников). Представителем прогестинов является прогестерон, который вырабатывается в желтом теле яичников. Небольшое количество женских половых гормонов вырабатывается в организме мужчин.
Ткани, чувствительные к действию эстрогенов, делятся на 2 группы: половые органы и неполовые органы.
Действие женских половых гормонов на половые органы
В половых органах женские половые гормоны способствуют развитию и функционированию этих органов и формированию вторичных половых признаков в период полового созревания.
В матке увеличивается рост железистого эпителия эндометрия и гладкой мускулатуры миометрия, усиливается васкуляризация органа.
Во влагалище увеличивается число слоев клеток, что является диагностическим критерием действия эстрогенов на организм.
В молочной железе эстрогены стимулируют рост протоков, прогестерон – рост железистой ткани.
Действие женских половых гормонов на неполовые органы
В неполовых органах эстрогены оказывают также характерное действие.
ЦНС, гипоталамус, гипофиз – под влиянием гормонов происходит формирование типичного полового поведения, инстинкта, психики женщины.
Кости, хрящи, гортань – эстрогены способствуют формированию характерного «женского» типа скелета, гортани и голоса. Эстрогены ускоряют окостенение эпифизов, где находятся зоны роста кости, поэтому, если у девочки в период полового созревания образуется мало эстрогенов, замедляется окостенение эпифизов, и в этом случае девочка может иметь необычно высокий рост. У взрослых женщин при продолжительном введении эстрогенов или их избыточном образовании в организме происходит интенсивное обызвествление костей, и могут исчезать полости, в которых находится костный мозг, что приводит к развитию анемии.
Кожа – эстрогены способствуют росту волос по женскому типу, тормозят рост волос на коже, снижают секреторную активность сальных желез (понижают сальность кожи).
Печень – эстрогены стимулируют синтез специфических белков печени: ангиотензиногена, способствующего повышению артериального давления, и некоторых факторов свертывания крови (II, VII, IX, X). Поэтому при избытке эстрогенов в организме наблюдается склонность к гипертонии и тромбозам.
Кроме этого, эстрогены, воздействуя на печень, увеличивают образование в ней липопротеинов очень низкой плотности (ЛПОНП) и липопротеинов высокой плотности (ЛПВП). ЛПОНП на 50 % состоят из триглицеридов (нейтрального жира), из печени они через кровь доставляются в жировую ткань, где жир откладывается. Поэтому у женщин мышцы всегда покрыты слоем подкожного жира. ЛПВП уменьшают концентрацию холестерина в крови, способствуют его выведению из организма. Поэтому женщины реже, чем мужчины, заболевают атеросклерозом и инфарктом миокарда.
Жировая ткань – в ней эстрогены и прогестерон увеличивают синтез жира, тормозят его расщепление, способствуют формированию типично женских жировых отложений.
Почки – эстрогены способствуют задержке натрия в организме, прогестерон усиливает потерю натрия с мочой. Поскольку при беременности образуется много прогестерона, натрий усиленно теряется организмом, отсюда – тяга к соленой пище.
Мужские половые гормоны
Мужские половые гормоны (андрогены) представлены тестостероном (рис. 13. и андростероном. Они образуются в семенниках, коре надпочечников, предстательной железе. Небольшое количество андрогенов синтезируется у женщин в яичниках.
Как и женские половые гормоны, андрогены действуют не только на половые, но и на неполовые органы.
Действие мужских половых гормонов на половые органы
В половых органах мужские половые гормоны оказывают андрогенное действие, то есть способствуют развитию и функционированию этих органов и формированию вторичных половых признаков в период полового созревания.
Действие мужских половых гормонов на неполовые органы
В неполовых органах андрогены обладают генерализованным анаболическим действием, то есть стимулируют синтез нуклеиновых кислот, белка, задерживают в организме азот и кальций, усиливают синтез фосфолипидов мембран.
ЦНС, гипоталамус, гипофиз – под влиянием андрогенов происходит формирование типичного полового поведения, инстинкта и психики мужчины, то есть образуются поведенческие особенности мужского пола. Андрогены влияют на развитие мозга. Если во внутриутробном периоде в критические стадии развития и дифференцировки мозга развивается недостаточность андрогенов, то в будущем у этого юноши или мужчины могут возникнуть варианты половой ориентации. Избыток андрогенов в организме способствует агрессивности.
Кости, хрящи, гортань – андрогены способствуют формированию характерных физиологических особенностей мужского скелета, гортани, голоса, усиливают отложение фосфорно-кальциевых солей в эпифизарных зонах роста. Чрезмерная выработка гормонов может приводить к преждевременному заращению эпифизов и развитию низкорослости.
Мышцы – андрогены увеличивают мышечную массу и силу, создают характерную рельефность мышц.
Кожа – андрогены обладают стимулирующим действием на сальные железы, повышая сальность кожи, усиливают пигментацию кожи (солнечный загар), увеличивают рост волос на лице и теле, способствуют росту волос по мужскому типу. Избыток гормонов может привести к облысению.
Жировая ткань – андрогены ускоряют расщепление жира в жировой ткани, тормозят его синтез.
В печени и почках андрогены резко увеличивают синтез белка, в кроветворных органах усиливают эритропоэз.
Анаболические стероиды
На основе мужских половых гормонов синтезированы аналоги этих соединений – анаболические стероиды, обладающие максимальной анаболической активностью и минимальной – андрогенной. Первоначально анаболические стероиды широко применяли для откорма скота. Однако анаболические стероиды очень плохо метаболизируют в организме животных и не разрушаются при термической обработке пищи. Поэтому, попадая с мясом в организм человека, анаболические стероиды вызывали тяжелые поражения печени, в том числе опухоли, поскольку продукты превращения этих соединений являются канцерогенами.
В настоящее время применение анаболических стероидов в практике животноводства уменьшилось. Однако некоторые спортсмены продолжают применять этих средства для повышения спортивных результатов. Тем не менее, установлено, что даже относительно кратковременное (в течение 2 лет) применение анаболиков в возрастном периоде с 18 до 26 лет (кроме перечисленных опасностей для здоровья спортсмена) может привести у мужчин к ранней импотенции, а у женщин – к раку молочной железы.
Небольшие дозы анаболических стероидов применяют в лечебной практике у лиц после 35 лет при тяжелых травмах, инфаркте миокарда, после операций для ускорения заживления ран, увеличения массы тела и улучшения аппетита при истощении.
Центральная регуляция эндокринной системы
Гормоны оказывают многообразное биологическое действие на организм. Синтез самих гормонов и выделение их в кровь, в свою очередь, регулируются потребностями организма. О потребностях организма сообщают импульсы, идущие от рецепторов по афферентным нервным волокнам в ЦНС. Там информация перерабатывается, и по эфферентным нервным волокнам импульсы идут на периферию. Однако нервная регуляция не охватывает функции всех клеток организма, поэтому дополняется гормональной регуляцией. Местом, где соединяются нервная и гормональная регуляции, является гипоталамус.
Нервные импульсы, идущие из ЦНС, приводят к образованию в гипоталамусе коротких пептидов, которые называются либеринами и статинами. Эти пептиды синтезируются в очень небольшом количестве и по системе портального кровообращения гипофиза переносятся к его клеткам (аденогипофизу). Здесь под влиянием либеринов активируется, а под влиянием статинов тормозится синтез тропных гормонов гипофиза. Выделяясь в кровоток, тропные гормоны достигают периферических эндокринных желёз, и там способствуют синтезу и выделению в кровь гормонов, которые и оказывают своё биологическое действие.
Гормоны гипофиза
В передней и средней доле гипофиза (аденогипофиз) образуются тропные гормоны. Задняя доля гипофиза (нейрогипофиз) только секретирует гормоны (вазопрессин и окситоцин), которые синтезируются в ядрах гипоталамуса.
Передняя доля гипофиза
АКТГ – адренокортикотропный гормон, или кортикотропин. Действует, главным образом, на пучковую зону коры надпочечников, где образуются, в основном, глюкокортикоиды. Кроме того, АКТГ усиливает расщепление гликогена в печени и жиров – в жировой ткани.
ТТГ – тиреотропный гормон, или тиреотропин. Регулирует развитие и функционирование щитовидной железы, синтез и секрецию в кровь тиреоидных гормонов.
ГТГ – гонадотропные гормоны, или гонадотропины. К ним относятся фолликулостимулирующий гормон (ФСГ, или фоллитропин) и лютеинизирующий гормон (ЛГ, или лютропин). ФСГ вызывает созревание фолликулов в яичниках у женщин и сперматогенез у мужчин. ЛГ стимулирует у женщин секрецию эстрогенов и прогестерона, вызывает образование желтого тела в яичниках, а у мужчин – секрецию тестостерона.
ЛТГ – лактотропный гормон, или пролактин. Стимулирует развитие молочных желез и лактацию у женщин, способствует формированию родительских инстинктов; у мужчин снижает половую потенцию.
Липотропные гормоны (липотропины) – оказывают жиромобилизующее действие (увеличивают распад жира).
СТГ – соматотропный гормон, или соматотропин, иначе называется «гормон роста». Особенностью гормона является его сильно выраженная видовая специфичность. Это значит, что СТГ животных не действует на человека.
Стимуляторами секреции гормона являются:
1. сон, особенно в первые часы после засыпания (если ребёнок мало спит, он плохо растет);
2. холод (в целом, северяне выше южан);
3. стресс (если ребенка ограждать от нормальных повседневных стрессов, он будет отставать в росте);
4. физическая нагрузка (в целом, спортсмены выше лиц, избегающих регулярных физических нагрузок).
Ткани-мишени для СТГ – все клетки организма.
1. Анаболическое. В клетках СТГ увеличивает синтез ДНК, РНК и белка, стимулирует рост костей (остеогенез), хрящей (хондрогенез) и мягких тканей, регулирует процессы роста и развития скелета и всего организма, приводит к увеличению размеров тела. Хрящевая ткань эпифизов наиболее чувствительна к действию СТГ, за счет этого происходит рост трубчатых костей в длину.
2. Диабетогенное. В печени СТГ активирует глюконеогенез (через стимуляцию секреции глюкагона). В мышцах и жировой ткани СТГ уменьшает проницаемость мембран для транспорта аминокислот в клетку. При избытке СТГ повышается концентрация глюкозы в крови и развивается инсулинорезистентность периферических тканей, т.е. соматотропный диабет.
3. Липолитическое. У детей в период интенсивного роста отсутствуют жировые отложения, так как в жировой ткани СТГ усиливает распад жира до жирных кислот. Жирные кислоты поступают в кровь и утилизируются в тканях. При избытке СТГ в крови значительно увеличивается концентрация жирных кислот, и они усиленно используются печенью по 2 направлениям:
• на синтез жира (поэтому при избытке СТГ развивается жировое перерождение печени);
• на бета-окисление, в результате чего образуется ацетил-КоА, который используется на образование кетоновых тел; поэтому при избытке СТГ повышается концентрация кетоновых тел в крови.
Патология
При недостатке выработки СТГ (гипофизарная карликовость, или нанизм) отмечается пропорциональное недоразвитие всего тела, низкий рост, но, в отличие от кретинизма, нет признаков деформации скелета и умственной отсталости.
Гиперсекреция СТГ возникает при опухолях аденогипофиза. Если такое состояние развивается в детском возрасте, до завершения окостенения скелета, наблюдается гигантизм, признаками которого являются чрезмерный рост скелета и непропорционально длинные конечности. Если гиперсекреция СТГ возникает у взрослых, то есть после завершения роста скелета, наблюдается акромегалия. Это заболевание характеризуется непропорционально интенсивным ростом отдельных частей скелета (кистей, стоп, подбородка, надбровных дуг, носа), разрастанием мягких тканей лица (губ, носа, языка), а также увеличением желез внутренней секреции, что может сопровождаться их гиперфункцией.
Средняя доля гипофиза
МСГ – меланоцитостимулирующие гормоны, или меланотропины. Увеличивают количество пигментных клеток (меланоцитов) и стимулируют выработку пигмента меланина в коже, радужке и сетчатке глаза.
Задняя доля гипофиза
Окситоцин и вазопрессин лишь условно относят к гормонам задней доли гипофиза, поскольку они синтезируются в особых нейронах гипоталамуса (в супраоптическом и паравентрикулярном ядрах). По отросткам нейронов эти гормоны поступают в заднюю долю гипофиза, где депонируются и откуда непосредственно выделяются в кровь.
Окситоцин является стимулятором гладкой мускулатуры матки при родах.
Вазопрессин, или антидиуретический гормон, вызывает сокращение гладкой мускулатуры сосудов, что приводит к сужению сосудов и повышению артериального давления. Помимо этого, вазопрессин оказывает мощное антидиуретическое действие – стимулирует обратное всасывание (реабсорбцию) воды в почках и уменьшает объем выделяемой мочи. При атрофии задней доли гипофиза развивается несахарный диабет – заболевание, при котором наблюдается выделение чрезвычайно больших количеств жидкости с мочой (10 – 20 л в сутки).
Использование гормонов в медицине
Гормоны в медицине применяются, в основном, по следующим направлениям.
1. Заместительная терапия: гормоны как лекарственные препараты используются при гипофункции эндокринных желез.
2. Использование механизмов действия гормонов на биохимические процессы и функции.
Например, окситоцин используют для стимуляции родовой деятельности, адреналин – для повышения артериального давления, глюкокортикоиды – для лечения воспалений и как противоаллергическое средство, половые гормоны – для лечения некоторых гормональнозависимых опухолей (эстрогены – для лечения рака предстательной железы, андрогены – для лечения рака молочной железы).
3.Использование аналогов гормонов: на основе женских половых гормонов созданы пероральные контрацептивы (противозачаточные средства), на основе мужских половых гормонов созданы анаболические стероиды.
Простагландины и другие эйкозаноиды
Название эйкозаноиды происходит от эйкозатетраеновой (арахидоновой) кислоты, из которой эти соединения образуются. Эйкозаноиды называют гормоноподобными веществами, а также местными или тканевыми гормонами, потому что, в отличие от истинных гормонов, которые образуются в одних органах (эндокринных железах), а действуют в других (тканях-мишенях), эйкозаноиды действуют там же, где и синтезируются.
Синтез эйкозаноидов
Эйкозаноиды образуются из арахидоновой кислоты, которая отщепляется от фосфолипидов мембран под действием фосфолипазы А2. Арахидоновая кислота может превращаться по 2 путям (рис. 14. : циклооксигеназному, главным ферментом которого является циклооксигеназа (простагландинсинтетаза), и липоксигеназному, с участием липоксигеназы. В результате циклооксигеназного пути превращения арахидоновой кислоты образуются простагландины, простациклины и тромбоксаны. В липоксигеназном пути синтезируются лейкотриены. Ингибиторы указанных ферментов применяются для уменьшения синтеза эйкозаноидов в тканях.
Лейкотриены – участвуют в воспалении, аллергии, иммунитете, привлекают лейкоциты в очаг воспаления, сужают бронхи, увеличивают секрецию бронхиальной слизи.
Простациклины – расширяют сосуды, снижают артериальное давление, препятствуют агрегации (слипанию) тромбоцитов, тем самым препятствуют тромбозам.
Тромбоксаны – способствуют слипанию тромбоцитов, тем самым способствуют тромбозам. Сильнее всех соединений сужают сосуды. Соотношение простациклин / тромбоксан в стенке сосудов имеет большое значение в развитии тромбозов.
Простагландины
Простагландины синтезируются во всех клетках, кроме эритроцитов. Разрушаются простагландины в организме очень быстро (через 20 мин), и продукты их распада выводятся с мочой.
Общим для действия простагландинов является то, что они, в основном, усиливают действие других гормонов через стимуляцию деятельности эндокринных желёз (гипофиз, щитовидная железа, поджелудочная железа, надпочечники).
Вместе с тем, различают 2 класса простагландинов: простагландины Е (PG E), растворимые в эфире, и простагландины F (PG F), растворимые в фосфатном буфере. Каждый из классов делится на подклассы, обозначаемые индексом, например, PG E1, PG E2, и т.д., и буквами греческого алфавита, например, PG F2a.
Действие простагландинов Е
1. Тормозят распад жира и гликогена.
2. Являются тканевыми факторами воспаления: вырабатываются в большом количестве в очаге воспаления, увеличивают проницаемость сосудов и клеточных мембран при воспалении, расширяют капилляры. PG E являются сильными пирогенами (повышают температуру тела). Аспирин является ингибитором синтеза простагландинов, поэтому снижает температуру тела.
3. Вызывают пульсирующие головные боли, которые снимаются через 20 мин после приёма аспирина.
4. Расширяют сосуды, снижают артериальное давление, поэтому применяются при гипертонии.
5. Расширяют бронхи, поэтому применяются для лечения бронхиальной астмы.
6. Снижают секрецию HCl в желудке, препятствуют развитию язв, поэтому применяются при язве желудка. Аспирин и глюкокортикоиды уменьшают образование простагландинов, тормозящих секрецию HCl, поэтому длительное применение глюкокортикоидов или неправильный приём аспирина способствуют образованию язв.
7. В почках увеличивают выделение (объём) мочи и натрия.
Действие простагландинов F
1. Стимулируют перистальтику кишечника.
3. В матке стимулируют гладкую мускулатуру, поэтому применяются для прерывания беременности и как стимулятор родовой деятельности.
Источник статьи: http://coollib.net/b/247451/read